用户文章一区,12分 | 非编码tRFs如何研究?Developmental Cell项目文章给您答案!
发布时间:2024-04-10 10:12 | 点击次数:
2023年12月18日,湖南大学生物学院于峰教授课题组在国际知名学术期刊Developmental Cell(IF=11.8/Q1)发表了题为“The FERONIA-YUELAO module participates in translational control by modulating the abundance of tRNA fragments in Arabidopsis”的研究论文,揭示拟南芥受体激酶FERONIA(FER)如何调节tRFs的丰度以抑制全局mRNA翻译。研究发现FER通过直接磷酸化tRNA结合蛋白YUELAO(YL)来调节tRF丰度,以调节其功能。FER和YL的下调抑制tRNA的胞嘧啶-5-甲基化和2′-O-甲基化修饰,从而增加了tRF的丰度。此外,还发现YL是FER信号传导的重要遗传下游靶点,敲低特定tRF部分挽救了FER和YL突变体的根毛生长缺陷。文章揭示了tRF的丰度和调节机制,以及它们在抑制植物翻译中的作用。
文章中测序技术RIP-seq,tsRNA(tiRNA&tRFs)测序,和LC-MS/MS核酸修饰检测(均由云序生物提供)



标题:The FERONIA-YUELAO module participates in translational control by modulating the abundance of tRNA fragments in Arabidopsis
发表时间:2023年12月18日
发表期刊:Developmental Cell
影响因子:IF=11.8/Q1
研究方法:tsRNA(tiRNA&tRFs)测序,RIP-seq,核酸修饰检测LC-MS/MS(均由云序生物提供)
研究摘要
长tRF在反密码子区域产生,而短 则在 D 或 T 区域发生切割时产生。tRNA 片段 (tRF) 是最近发现的一类小非编码 RNA,由成熟的 tRNA 生成。根据切割位点可分为长tRF(30-35 个核苷酸 )和短tRF(15-29 nt)。迄今为止,植物中 tRF 丰度的调控及其功能机制尚不清楚。作者研究了拟南芥受体激酶 FERONIA (FER) 如何调节 tRF 的丰度来抑制整体 mRNA 翻译。作者证明 FER 通过直接磷酸化 tRNA 结合蛋白 YUELAO (YL) 来调节 tRF 丰度,从而调节其功能。FER 和 YL 的下调可阻止 tRNA 通过胞嘧啶 5-甲基化和 20-O-甲基化进行修饰,从而增加 tRF 丰度。此外,作者还发现,YL 是 FER 信号传导的重要遗传下游靶标,敲除特定 tRF 可以部分挽救 fer 和 yl 突变体的根毛生长缺陷。作者的研究结果揭示了 tRF 的丰度和调控机制及其在抑制植物翻译中的作用。
技术路线

*红色部分技术服务云序提供
研究结果
1、FER 介导抑制翻译的某些 5’tRF 的丰度
考虑到 FER 在 RNA 代谢中的多重作用,作者推断该蛋白质可能通过影响小 RNA (sRNA) 的丰度来调节翻译。因此,作者通过tsRNA(tiRNA&tRFs)测序数据分析9天龄野生型(WT;Col-0)和 fer-4(FER 无效突变体)拟南芥 (Arabidopsis thaliana) 幼苗中的 sRNA(长度<40 nt)。散点图分析显示,与WT相比,fer-4突变体积累了不同水平的三种类型的sRNA(mRNA片段、microRNA和tRF)。值得注意的是,所得到的测序文库在 fer-4 中比在 WT 中含有更丰富的 20-35 nt tRF;这些分子主要源自 tRNA 的 5' 末端(短 20-29 nt和长 30-35 nt 5' tRF)。作者列出了来自不同 tRNA 同种型的代表性 5' tRF,其丰度在 fer-4 突变体中显着上调(>1.5 倍;padj < 0.05)。作者还列出了 fer-4 中的所有 tRF 及其丰度。重点关注五个 5' tRF,因为它们相对于其他 tRF 特别丰富:5' tRFHisGTG(25 nt;增加 6.3 倍)、5' tRFGly-TCC(30 nt;6.0 倍)、5' tRFGlu-CTC(29 nt) ;5.95 倍)、5' tRFAla-AGC(20 nt;2.6 倍)和 5' tRFSer-AGA(22 nt;2.6 倍),下文中作者将其分别称为 His25、Gly30、Glu29、Ala20 和 Ser22。
作者通过在原生质体中进行瞬时双荧光素酶测定来研究这些 tRF 是否会导致 fer-4 突变体中出现的翻译缺陷。当作者使用萤火虫荧光素酶 (LUC) 报告基因转化从 WT 或 fer-4 制备的原生质体时,作者测量到 fer-4 相对于 WT 的相对 LUC 活性较低,这与之前的发现一致。为了研究5’ tRF在这翻译抑制中的作用,作者使用了短串联靶模拟物(STTM ) 方法敲低 (KD) fer-4 原生质体中的单个 5' tRF。发现降低单个 tRF Gly30、Glu29 和 Ala20 的丰度部分挽救了 fer-4 原生质体中出现的翻译缺陷,且对报告基因 mRNA 水平几乎没有影响。Ser22 的 敲低仅具有适度的效果;然而,His25 的敲低(用作阴性对照)对 LUC 翻译没有影响。当所有四种 tRF(Gly30、Glu29、Ala20 和 Ser22)一起被敲除时,fer-4 中的翻译缺陷得到更大程度的挽救。这些结果表明 FER 的功能的丧失可能是 5' tRF 丰度发生特定变化的原因,从而导致 fer-4 突变体的翻译缺陷。接下来作者使用体外小麦胚芽翻译系统来测试 5' tRF 对 LUC mRNA 翻译的影响。作者将合成 tRF Gly30、Glu29、Ala20 和 Ser22 添加到翻译反应中,并测量所得的 LUC 活性。所有四种合成 tRF 一起添加或单独添加 Ala20 tRF 会抑制 LUC 翻译。相比之下,tRF Glu29 和 Gly30 单独对该系统中的 LUC 翻译没有影响。这些数据与 Ala20 抑制小麦胚芽系统翻译的发现一致。
作者使用人工 microRNA (amiRNA) 在 WT 拟南芥原生质体中分别过表达 tRF Gly30、Glu29、Ala20 和 Ser22。所有四种 tRF 的过表达 (OE) 对 LUC 产生了更强的影响,与单独过表达 Ala20 时相比,翻译水平下降,并且在过表达 Glu29 或 Gly30 tRF 时也观察到一些翻译抑制,这与小麦胚芽系统中的发现相反。这些 tRF 均未引起 LUC 转录本丰度发生任何可测量的变化,支持这些 tRF 在翻译水平发挥作用的假设。除了从质粒中过表达每个 tRF 之外,作者还将合成的 tRF 直接转染到原生质体中,并获得了类似的 LUC 翻译结果。这些差异表明 Gly30 和 Glu29 通过未知机制抑制全局翻译。
作者还更详细地研究了四种 tRF 的水平。使用定制 sRNA TaqMan 探针对 tRFs 进行逆转录定量 PCR (RT-qPCR),证实这四种 tRF 的水平在 fer-4 中显着高于 WT。作者使用两种核酸修饰探针通过 RNA 凝胶印迹分析进一步证实了 fer-4 中这 4 个 5' tRF 的高丰度。作者使用 5' tRFPhe-AGC(20 nt;fer-4 与 WT,0.078 倍;p > 0.05)作为阴性对照,因为其丰度不受 fer-4 突变的影响。总之,这些结果表明 FER 调节具有翻译功能的某些 5' tRF 的丰度。

图 1. 特定 FER 介导的 5’ tRF 的丰度调节蛋白质合成
(A)散点图显示从野生型 (WT) Col-0(x 轴)或 fer 分离的样品中 tRF 的丰度(以百万分之一计)
(B)tRNA 及其衍生 tRF 二级结构的预测。图中显示了两类 5’ tRF,其丰度在 fer-4 突变体中增加:源自 D 环裂解的短 tRF;,反密码子环裂解产生的长 tRF。
(C)源自不同 tRNA 同种型的代表性tRF,其丰度在 fer-4 突变体中显着上调
(D)顶部双荧光素酶 (dual-luc) 报告基因测定显示,特定 tRF 的敲低可部分挽救转染 fer-4 原生质体中的 35S:LUC 报告基因的荧光素酶活性,其中用空质粒转染的原生质体作为模拟对照。底部的 qPCR 检测显示特定的 tRF 对报告基因的转录水平没有显着影响。
(E)使用小麦胚芽系统进行的体外翻译测定显示总 tRF(Ala20、Ser22、Glu29 和 Gly30)和 Ala20 抑制翻译。
(F)顶部双 luc 报告基因测定显示,特定 tRF 的过表达会抑制 WT 原生质体中转染的 35S:LUC 报告基因的荧光素酶活性,其中 His25 作为阴性对照,用空质粒转染的原生质体作为模拟对照。底部,qPCR 检测显示特定 tRF 的下调对报告基因的转录水平没有显着影响。
(G)顶部双 luc 报告基因测定显示,特定 tRF 抑制 WT 原生质体中转染的 35S:LUC 报告基因的荧光素酶活性,其中 His25 作为阴性对照,用随机 RNA 转染的原生质体作为模拟对照。,底部,qPCR 检测显示特定 tRF 的下调对报告基因的转录水平没有显着影响。
(H)qPCR 显示 fer-4 中 Ala20、Ser22、Glu29 和 Gly30 tRF 的表达显着上调。
(I-M) WT 和 fer-4 幼苗中特定 tRNA 及其相应 tRF 的 Northern 印迹分析。,50 tRFPhe-AGC (Phe20) (20 nt) 在 fer-4 中未上调 (padj > 0.05),并用作阴性对照。
(N) 使用 ImageJ 对 (I)–(M) 中的 tRF 和 tRNA 水平进行定量。
2、FER 与预测的 RBP YL 发生物理关联并使其磷酸化
最近的研究表明,与非 RBP 相比,RNA 结合蛋白 (RBP) 在本质无序区域 (IDR) 中富集。使用之前筛选的 FER 相互作用蛋白的数据,作者注意到一种相互作用,由 At5g11090 编码的未知功能蛋白YUELAO1 (YL1)。在拟南芥中鉴定出两个 YL1 同源物,它们也包含广泛的 IDR。作者研究了 YL1、YL2 和 YL3 的表达模式和定位。系统发育分析表明,YL 是植物特异性的,可能起源于被子植物与裸子植物的分化之前。这三个 YLs 在体外均与 FER 的胞质结构域(FERCD,氨基酸 469-895)相互作用。使用免疫共沉淀 (coIP) 测定,作者确定 FER 在体内与 YL 蛋白相互作用。作者还在 LUC 互补测定中观察了 FER-NLuc 和 CLuc-YL1 之间的相互作用(荧光素酶分为 N 端和 C 端片段)。此外,作者还发现 YL1 和 YL2 可以与 FER 的亲属的几个 CrRLK1L 家族成员相互作用。总的来说,这些结果表明 FER 和几种相关蛋白质与 YL 发生物理相互作用。
作者研究了 FER 介导的底物磷酸化,结果表明,当通过 SDS-PAGE 分离时,活性 FER 激酶而非激酶死亡变体 FER-CDK565R 会导致 YL1、YL2 和 YL3 的迁移率发生变化。作者鉴定了 YL1 中的 6 个氨基酸残基,它们受到 FER 介导的磷酸化作用。所有磷酸化位点似乎都位于与其他植物物种相对保守的残基处。作者同时将所有六个已识别的 YL1 磷酸化位点突变为丙氨酸残基 (YL1mutA),以完全阻止 YL1 磷酸化;事实上,YL1mutA-His 在体外没有被 FER-CD 磷酸化。
为了评估 YL1 是否在体内被 FER 磷酸化,作者使用泛抗 YLs 抗体对 WT 和 fer-4 幼苗的 YL 蛋白进行免疫沉淀,并使用两种针对磷酸苏氨酸残基的抗体检查其磷酸化状态。在 WT 中,RALF1 处理增强了 YL 的磷酸化水平,而无论 RALF1 处理如何,YL 在 fer-4 中仅表现出非常弱的磷酸化信号。此外,作者对来自 WT 和 FER-K565R fer-4 幼苗的 YL 蛋白进行免疫沉淀并检查了 YL 磷酸化状态。在 WT 中,RALF1 处理增强了 YL 的磷酸化水平;然而,无论 RALF1 处理如何,YL 在 FER-K565R fer-4 中都显示出微弱的磷酸化信号,与 fer-4 幼苗中看到的类似。虽然 YL 的磷酸化并不完全依赖于 FER,但与 WT 相比,fer-4 无效突变体和 FER-K565R fer-4 系严重损害了 YL 的磷酸化,表明 FER 的激酶活性在YL 的磷酸化。作者还生成了 YL1Myc 和 YL1mutA-Myc 转基因系,以评估 YL1 中磷酸化残基的贡献。 RALF1 促进 YL1-Myc 幼苗中 FER 介导的 YL1 磷酸化,而 YL1mutA-Myc 幼苗则呈现出更弱的磷酸化信号,无论 RALF1 处理如何。总之,这些结果表明 YL 直接与 FER 相互作用并被 FER 磷酸化。

图 2. FER 与 YL1 物理结合并磷酸化 YL1 (A) Y2H 测定显示 YL1 和 FER 之间的相互作用。
(A)使用含有 20 mM 3-氨基-1,2,4-三唑 (3-AT) 的 SD/-Ade/-Leu/-His 选择培养基来测试蛋白质-蛋白质相互作用。
(B)使用重组 His-TF-YL1 和 FER-CD-S 或 His-TF 作为对照进行 His Pull-down 测定。分别通过抗His和抗Stag抗体检测到指定的His标签和S标签。
(C)CoIP 测定。,分别使用抗 FLAG 和泛抗 YL 抗体鉴定免疫沉淀 FER-FLAG 和共免疫沉淀 YL。
(D)荧光素酶互补测定显示本塞姆氏烟草叶子中 CLuc-YL1 和 FER-NLuc 之间的相互作用。
(E)FER 对 FER 和 YL1 的体外磷酸化测定。标出了磷酸化和去磷酸化的重组 FER-CD-S 和 YL1-His。,使用抗S标签抗体检测FER-CD-S,使用抗His抗体检测YL1-His。考马斯亮蓝 (CBB) 染色显示为上样对照。
(F)WT 和 fer-4 幼苗的体内磷酸化测定。,pThr/Tyr 和 pSer 抗体用于检测磷酸化的 YL。,对于 RALF1 处理,将 1 周龄的 Col-0 和 fer-4 幼苗单独在半强度液体 MS 培养基中孵育或与 1 mMRALF1 一起孵育 1 小时。WT 和 fer-4 样品用碱性磷酸酶 (AP) 处理,以测试免疫印迹信号的特异性。使用泛抗 YLs 抗体作为上样对照。使用 ImageJ 进行磷酸化水平的量化,并显示在印迹的右侧。
(G)使用 WT 和激酶死亡 FER 点突变体 K565R 进行体内磷酸化测定。pThr/Tyr 和 pSer 抗体用于检测磷酸化的 YL。对于 RALF1 处理,将 1 周龄的 Col-0 和 FER-K565R fer-4 幼苗单独在半强度液体 MS 培养基中或与 1 mMRALF1 一起孵育 1 小时。,使用泛抗YLs抗体作为上样对照。,使用 ImageJ 进行磷酸化水平的量化,并显示在印迹的右侧。
(H)WT 和 YL1 点突变体的体内磷酸化测定。pThr/Tyr 和 pSer 抗体用于检测磷酸化的 YL1。,对于 RALF1 处理,将 1 周龄的 YL1-Myc 和 YL1mutA-Myc 幼苗单独在半强度液体 MS 培养基中或与 1 mM RALF1 一起孵育 1 小时。使用抗肌动蛋白抗体作为上样对照。,使用 ImageJ 进行磷酸化水平的量化,并显示在印迹的右侧。
3、YL 是一种 tRNA 结合蛋白
作者研究了 YL 是否起到直接结合 RNA 的 RBP 的作用。作者进行了高通量 RNA 免疫沉淀测序 (RIP-seq),结果表明 YL 可以直接识别多种类型的 tRNA。作者使用 MEME41 寻找 YL 结合的 tRNA 同工受体中共有的顺式元件,并鉴定了两个 tRNA 基序(作者分别表示为 M1 和 M2)M1 位于 TJC 茎环中,而 M2 位于 D 茎环中。作者确认了 YL1 与这两个基序中的每一个之间的相互作用。作者进一步测试了 YL1 与缺乏任一基序的 tRNA 中与 M1 或 M2 大致位置相同的序列之间的相互作用潜力。作者确定 YL1 不能直接与这些序列相互作用。还观察到任一基序的不同突变都会损害它们与 YL1 的相互作用。这些体外结果表明 YL1tRNA 结合是序列依赖性的。
接下来,作者通过 RIP-qPCR 在 WT 和 yl1 yl2 yl3 幼苗上测试了 tRNA和 YL 之间的相互作用(图 3F 和 S4C)。作者确定并非所有含有 M1 和/或 M2 基序的 tRNA 同工受体都能在体内与 YL 发生免疫沉淀(YL 对 RIP-seq 数据中缺失的 tRNA 的结合能力较弱或无法检测到),表明 YL 的偏好体内特定 tRNA 同工受体。这些结果表明,tRNA结合蛋白YL可能具有复杂的RNA结合能力,这可能需要其他蛋白质来特异性结合某些tRNA并通过RNA二级结构赋予靶标识别能力。
作者假设 FER 调节 YL 的 RNA 结合能力。因此,作者检查了 WT 和 fer-4 中的 YLs-tRNA 相互作用:作者观察到,相对于 WT,fer-4 突变体中 YLs 对 tRNAAla、tRNAGly 和 tRNAGlu 的亲和力降低。

图 3. YL 是 tRNA 结合蛋白
(A)左图,饼图显示通过 RIP-seq 鉴定的各个 YL 结合 tRNA 同工受体的富集。,右图,富集的 tRNA 基序 M1 和 M2。
(B)体外电泳迁移率变动分析 (EMSA) 显示重组 YL1 可以直接结合 tRNA 基序 M1 和 M2。
(C)体外EMSA显示重组YL1不能直接结合序列S1和S2,序列S1和S2与缺少M1和/或M2的tRNA中的基序M1和M2位于相同位置。
(D-E)体外 EMSA 显示基序 M1 和 M2 中的不同突变会损害 YL1 的结合。,表 S4 中提供了 mut1-4 的序列。,使用 ImageJ 进行相互作用强度的量化并显示在 (D) 中。
(F) 体内 RIP-qPCR 显示,RIP-seq 未检测到的 YL 与 tRNA 的结合能力较弱或无法检测,具体取决于 tRNA。
(G-H)链霉亲和素磁性 RNA 蛋白下拉测定显示 fer-4 突变损害了 YL 的 RNA 结合能力。,tRNAHis 未在 tRNA RIP-seq 数据中被识别,并作为阴性对照。,YL 强度的量化使用 ImageJ 进行,如 (H) 所示。
(I-J) 链霉亲和素磁性 RNA 蛋白下拉测定显示 FER-K565R fer-4 转基因系也会损害 YL 的 RNA 结合能力。使用 ImageJ 进行蛋白质强度的量化并显示在 (J) 中。
(K–N) YL1mutA 表现出较弱的 RNA 结合能力。,与YL1相比,YL1mutD表现出更强的RNA结合能力。,使用 ImageJ 进行相互作用强度的量化,如 (L) 和 (N) 所示。
4、YL 与 FER 一样,调节特定 5' tRF 的丰度
作者研究了 YL 是否也调节 fer-4 水平增加的特定 5' tRF 的丰度。因此,作者开发了一组 yl 双突变体和两个独立的 yl1 yl2 yl3 三突变体。与 fer-4 类似,与 WT 相比,yl1 yl2 yl3 三重突变体(9 天)的特征是三种类型 sRNA 的水平不同。作者确定,相对于 WT,yl1 yl2 yl3 三重突变体中水平显着改变的特定 tRF 主要源自 tRNA 的 5' 端,如 fer-4 中那样。作者创建了来自不同 tRNA 同种型的代表性 5' tRF 的列表,这些 tRF 在 yl1 yl2 yl3 突变体中显着上调(>1.5 倍;padj < 0.05)。值得注意的是,丰度发生显着变化的 5' tRF 在 fer-4 和 yl1 yl2 yl3 中都是相同的,其中一些 5' tRF 在每个突变体中表现出不同的丰度方向。FER 可能通过另一条不依赖于 YL 的途径调节 5' 种 tRF 的水平。
然后,作者研究了 yl1 yl2 yl3 是否也下调翻译。与 fer-4 类似,yl1 yl2 yl3 也表现出较低水平的多核糖体分数以及异常的 40S 和 80S 峰。
作者使用与之前在 yl1 yl2 yl3 原生质体中 KD 5' tRF 相同的 STTM 方法,测试了某些 5' tRF 是否会导致 yl1 yl2 yl3 中出现的翻译缺陷。与 fer-4 的结果类似,敲低单个 tRF Gly30、Glu29、Ala20 和 Ser22 部分挽救了 yl1 yl2 yl3 中出现的翻译缺陷,且对 LUC mRNA 水平没有可检测到的影响;然而,His25(阴性对照)对 LUC 翻译没有影响。当所有四个 tRF 都被敲除时,yl1 yl2 yl3 中的翻译缺陷也得到了更大程度的挽救。这些结果表明,YL 与 FER 一样,是 5' tRF 丰度和 mRNA 翻译的关键调节因子。
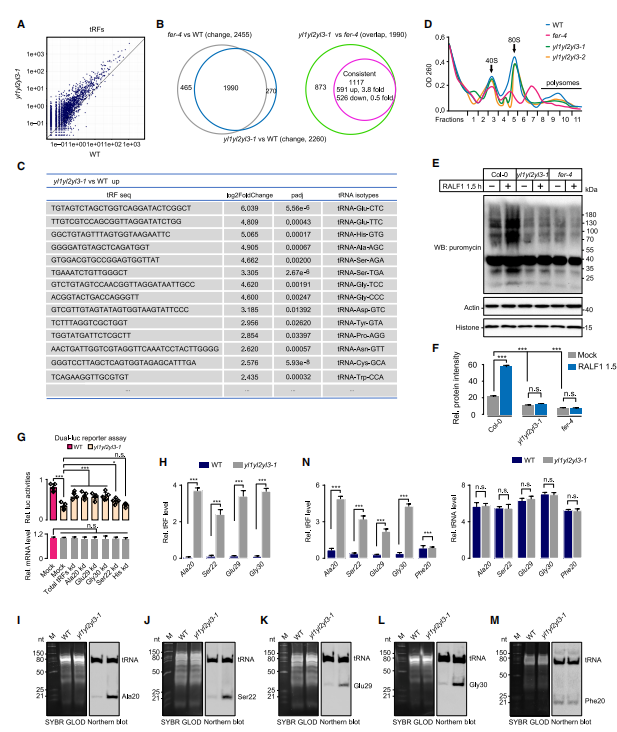
图 4. YL 与 FER 一样,调节特定 5’ tRF 的丰度和整体蛋白质合成
(A)散点图显示从 WT(x 轴)和 yl1 yl2 yl3 突变体分离的样品中 tRF 的丰度(以百万分之一计)
(B)Venn显示 fer-4 或 yl1 yl2 yl3 突变体中差异丰富的 5’ tRF 数量相对于 WT 之间的重叠程度。在两个突变体共有的 1,990 个差异丰富的 5’ tRF 中,1,117 个 5’ tRF 显示出一致的变化(591 个上调,526 个下调),平均上调 3.8 倍,而下调的 5’ tRF 中平均下调 0.5 倍。,
(C)源自不同 tRNA 同种型的代表性 50 个 tRF,与 WT 相比,这些 tRF 在 yl1 yl2 yl3 突变体中显着上调(padj:BH 调整后的 p < 0.05)。
(D)多聚体分析测定显示 WT、yl1 yl2 yl3 和 fer-4 中蛋白质合成的程度。
(E-F) 嘌呤霉素掺入测定显示 WT、yl1 yl2 yl3 和 fer-4 响应 1 mM RALF1 处理的总体蛋白质合成。,使用 ImageJ 进行蛋白质强度的定量,如 (F) 所示。
(G)顶部双荧光素酶 (dual-luc) 报告基因测定显示,特定 tRF 的敲低可部分挽救 yl1 yl2 yl3 原生质体中转染的 35S:LUC 报告基因的荧光素酶活性,其中用空质粒转染的原生质体作为模拟对照。底部,qPCR 检测显示特定 tRF 的敲低对报告基因的转录水平没有显着影响。
(H) qPCR 显示,相对于 WT,yl1 yl2 yl3-1 中特定 tRF 的丰度显着上调。
(I–N) 使用特定探针对 WT 和 yl1 yl2 yl3-1 中的特定 tRNA 和 tRF 进行 Northern 印迹分析。Phe20 在 yl1 yl2 yl3 (padj > 0.05) 中不受调节,用作阴性对照。(I)–(M) 中 RNA 强度的量化是使用 ImageJ 进行的,如 (N) 所示。
5、FER-YL 调节 tRNA 甲基化水平
接下来,作者探索 FER-YL 驱动的 5' tRF 丰度的可能分子基础。tRNA 修饰可调节 tRF 的产生。因此,作者测试了 tRNA 修饰在调节 tRNA 稳定性方面的可能贡献。为此,在体外合成了tRNAGly、tRNAGlu、tRNASer和tRNAAla转录本(未修饰);同时用特定的生物素探针从幼苗提取物中纯化了每种 tRNA(经过修饰)。将每种 tRNA(修饰的和未修饰的)与从 WT 幼苗中制备的粗酶提取物一起孵育后,作者观察到合成的 tRNA 转录本比从幼苗中纯化的 tRNA 产生更多的 tRF。基于这些发现,作者从 WT、fer-4 和 yl1 yl2 yl3 幼苗中纯化了 tRNA,并将它们完全消化至单个核苷,然后进行液相色谱-串联质谱 (LC-MS/MS) 核酸修饰检测 2'-O-甲基腺苷 (Am)、2'-O 甲基尿苷 (Um)、Cm、Gm、1-甲基金苷,(m1A)、N6 甲基腺苷 (m6A)、N4-乙酰胞苷 (ac4C)、m5C 和 7 甲基鸟苷 (m7G)等修饰含量。作者观察到,与 WT 相比,fer-4 和 yl1 yl2 yl3 突变体中的 Cm、Gm、m5C 和 ac4C 修饰水平较低(图 5C 和 5D),而 yl1 yl2 中 m7G、m1A 和 m6A 的水平增加yl3和fer-4。
先前的研究表明,tRNA 中较低的 Cm、Gm 和 m5C 水平可以导致 tRF的产生,这与作者的研究结果一致。因此,作者使用抗 m5C 抗体对从 9 日龄 WT、fer-4 和 yl1 yl2 yl3 幼苗提取的总 RNA 进行了免疫印记和斑点印记测定。结果与 LC-MS/MS 分析一致,相对于 WT,突变体中检测到的 m5C 水平较低。这些结果表明 FER-YL 在 tRNA 修饰中发挥作用。
为了在本研究中检查 FER-YL 介导的 5' tRF 丰度调节与全长 tRNA 水平之间的关系,作者检查了 tRNA 的丰度。作者观察到 WT 和突变体之间成熟 tRNA 水平没有差异。Northern 印迹分析还表明,敲除 FER 或 YL 似乎不会干扰全长 tRNA 的稳定性。最近的几项研究表明,tRF 丰度不一定与其相应 tRNA 丰度呈线性关系,表明“管家”tRNA 水平的调节和 tRF 水平的动态变化是复杂的。总之,这些结果表明 FER-YL 模块参与 tRNA 修饰。然而,YL 在 tRNA 甲基化中的作用以及 FER-YL 模块如何调节 tRNA 甲基化水平仍不清楚。
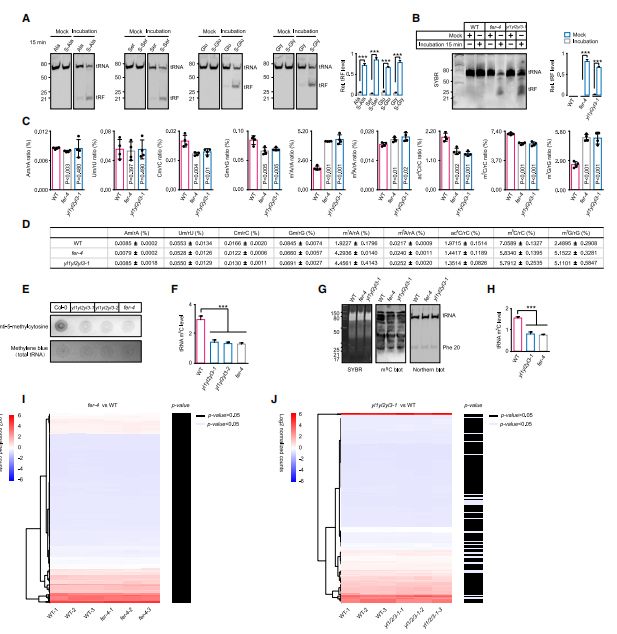
图 5. FER-YL 调节 tRNA 甲基化水平以调整 tRF 产生
(A) tRNA 裂解测定表明,合成的转录物产生比体内 tRNA 更多的 tRF。使用 ImageJ 进行 tRF 带强度的量化,如右图所示。
(B)tRNA 裂解测定显示 fer-4 和 yl1 yl2 yl3 从总 tRNA 池中产生比 WT 更多的 tRF。,使用 ImageJ 进行 tRF 带强度的量化,如右图所示。
(C-D) WT、fer-4 和 yl1 yl2 yl3 中 tRNA 修饰 Am、Um、Cm、Gm、m1A、m6A、ac4C、m5C 和 m7G 水平的定量。(E-F) 斑点印迹测定显示 yl1 yl2 yl3 和 fer-4 突变体中总 tRNAm5C 水平降低。,在用抗体探测之前,首先用亚甲蓝对 tRNA 斑点印迹进行染色,以确认样品的负载量相等。,m5C 水平的量化使用 ImageJ 进行,如 (F) 所示。,
(G-H) 免疫印迹显示 yl1 yl2 yl3 和 fer-4 中总 tRNA m5C 水平降低。,m5C 水平的量化使用 ImageJ 进行,如 (H) 所示。,
(I-J) tRNA 丰度(log2 标准化计数)的热图表示显示,通过 tRNA-seq 确定的 WT 和突变体中成熟 tRNA 的水平没有差异。
6、FER-YL 信号在植物繁殖和发育中发挥关键作用
yl双突变体比野生型植物产生更短的长角果和更少的种子,类似地,两个独立的yl1 yl2 yl3 三重突变体显示出严重的生殖缺陷。作者观察到 yl1 yl2 yl3 突变体的花粉管接收缺陷。yl双突变体和三突变体的根毛比WT短,并且yl1 yl2 yl3和fer-4都形成比WT更小的莲座丛。此外,YL在RALF1和脱落酸(ABA)信号反应以及对盐和甘露醇应激的反应中的作用与 FER 类似。
先前的一项研究表明,FER 调节植物 2 中 RHO 相关蛋白 (ROP2)的蛋白质合成,并且 FER-ROP2 信号传导调节烟酰胺腺嘌呤二核苷酸磷酸 (NADPH) 氧化酶活性以控制多种生理反应,这表明活性氧(ROS)的产生对于 FER 功能至关重要。作者确定 yl1 yl2 yl3 中的 ROS 爆发进程与 fer-4 中的相似。ROP 是否可能成为 YL 的目标。事实上,相对于 WT,yl1 yl2 yl3 中 ROP2、ROP4 和 ROP6 mRNA 的翻译较低。作者生成了多个 yl1 yl2 yl3 fer-4 四重突变体,发现它们的表型并不比 fer-4 更严重。总之,这些结果表明 YL 作为在 FER 信号传导中起作用的重要下游因子,并且 FER-YL 模块途径将此处提供的数据与之前确定的 FER-鸟嘌呤核苷酸交换因子(GEF)-ROP 途径相协调。
最后,为了证实 tRF 在 FER-YL 信号传导中发挥关键作用的观点,作者为 WT 背景中的五个 tRF 中的每一个生成了 OE 系。与 fer-4 和 yl 一样,Ala20-OE、Glu29-OE 和 Gly30-OE 植物表现出短根毛;Ser22-OE 的根毛也比 WT 短,和His25-OE(阴性对照)植物表现出与WT相同的根毛长度(图9E和9F)。此外,作者敲低了 yl1 yl2 和 fer-4 背景中的 tRF。作者确定 Ala20-kd yl1 yl2 和 Gly30-kd yl1 yl2 的根毛比 yl1 yl2 更长。与 fer-4 相比,Ala20-kd fer-4 和 Gly30-kd fer-4 表现出非常短的根毛,His25 的 KD 不能挽救 fer-4 或 yl1 yl2 的根毛生长缺陷。作者通过 Northern blot 分析确认了每个 tRF 的 OE 或下调 (KD)。这些数据表明,特定 tRF 的 KD 部分挽救了 fer 和 yl 突变体的根毛生长缺陷,并且正常的 tRF 丰度是 FER-YL 途径正常发挥作用所必需的。

图 6. YL 中的突变诱导与 fer-4 中相似的营养和繁殖表型
(A)yl 显示出与 fer-4 类似的生殖缺陷。
(B) 苯胺蓝染色的胚珠的落射荧光显微照片显示了 WT、fer-4 和 yl1 yl2 yl3 中雌配子体内生长的花粉管。
(C) WT 和突变体 4 天龄幼苗(上图)和 30 天龄植物莲座丛表型(下图)的根毛形态的代表性图像。
(D) WT、yl和fer-4中的结籽;,每行检查 10 个长角果。
(E) WT、yl和fer-4中的平均根毛长度;,测量每个基因型 8 至 10 个根的 50-120 个根毛。
全文总结
植物中的 RLK 类似于动物中的 G 蛋白偶联受体 (GPCR)。尽管之前的研究已经检验了 RLK 如何调节植物中的细胞活动,但本研究的结果以及之前发现的 FER 在选择性剪接和翻译中发挥关键作用。FER 是植物对多种非生物和生物胁迫作出反应的中心枢纽。重要的是,之前的研究已经说明了胁迫如何调节 tRFs 的丰度;然而,将这些不同的细胞外刺激与应激诱导的 tRF 表达联系起来的机制仍然未知。目前的研究结果表明,FERYL-tRF 模块是响应复杂环境信号而控制全局蛋白质生物合成的重要上游信号通路。我们的遗传数据表明,特定tRF的OE和KD影响幼苗的根毛生长,并导致土壤中的非繁殖和生长缺陷,这表明不同tRF的功能冗余。除了 tRF 之外,fer-4 和 WT 之间其他 RNA 种类的丰度也存在差异。这一发现表明 FER 信号传导在 sRNA 丰度动态和 sRNA 介导的转录或转录后调控中发挥着关键作用。FER 是一种 CrRLK1L 蛋白,参与与 RALF 信号传导相关的多种生理反应。yl1 yl2 yl3 三重突变体没有表现出与 fer-4 相同的表型,这表明 FER 不仅通过 YL调节 5’ tRF 水平或翻译,而且还通过另一个途径。FER 及其激酶活性在 YL 磷酸化中起主要作用,但 FER 不太可能是可以磷酸化 YL 的激酶。
相关产品
tsRNA(tiRNA&tRFs)测序
往期回顾
云序客户m6A高分文章|揭示组蛋白乙酰化与m6A修饰在眼部黑色素瘤发生中的共同作用机制
用户文章 IF=19.2|范先群院士团队利用m1A MeRIP-seq联合多组学测序揭示眼黑色素瘤调控新机制
云序客户| m6A MeRIP-seq助力揭示早发糖尿病表观调控新机制
客户文章|IF=10.6—甲状腺癌中m5C甲基转移酶NSUN2通过维持tRNA的稳定性促进密码子依赖性的致癌翻译
云序客户| MeRIP-seq+RIP-seq技术揭示 m6A 甲基化调控BMSCs成骨分化新机制
客户文章| Nature子刊 揭示了FMR1通过m6A修饰调控早期胚胎发育的分子机制
用户文章m6A专题|IF=9.8|m6A去甲基化酶ALKBH5缺乏会加重钴致神经退行性损伤
用户文章 1区 lncRNA m6A甲基化测序助力人脂肪干细胞成骨分化的调控机制研究
客户文章|1区,IF=9.995|m6A甲基化测序助力宫颈癌相关HPV病毒研究
用户文章IF=19.568|m5C修饰测序助力NSUN2调控病毒I型干扰素反应的机制研究
Nature 新发现:线粒体 m5C 修饰竟是肿瘤转移的元凶!
用户文章IF=14.9 1区:ac4C乙酰化调节人胚胎干细胞的自我更新
云序用户农口IF20+论文:植物mRNA存在ac4C新型修饰,对RNA稳定性及翻译产生重要影响
用户文章:m7G 甲基化参与调节心肌细胞增殖|新型RNA修饰研究
云序用户植物文章6连发:植物当中各类RNA甲基化测序该怎么发?
庆祝云序用户m1A、m6A、m5C RNA甲基化测序文章三连发




