用户文章|1区 IF=17.694:m6A MeRIP-seq 助力饥饿条件下的细胞自噬研究
发布时间:2022-10-26 09:27 | 点击次数:


发表日期:2022 年 10 月 4 日
客户单位:南方医科大学
研究方法:m6A MeRIP-seq、RIP-seq 、co-IP 、蛋白质谱、LC-MS/MS 核酸修饰整体水平检测、qPCR等
技术路线
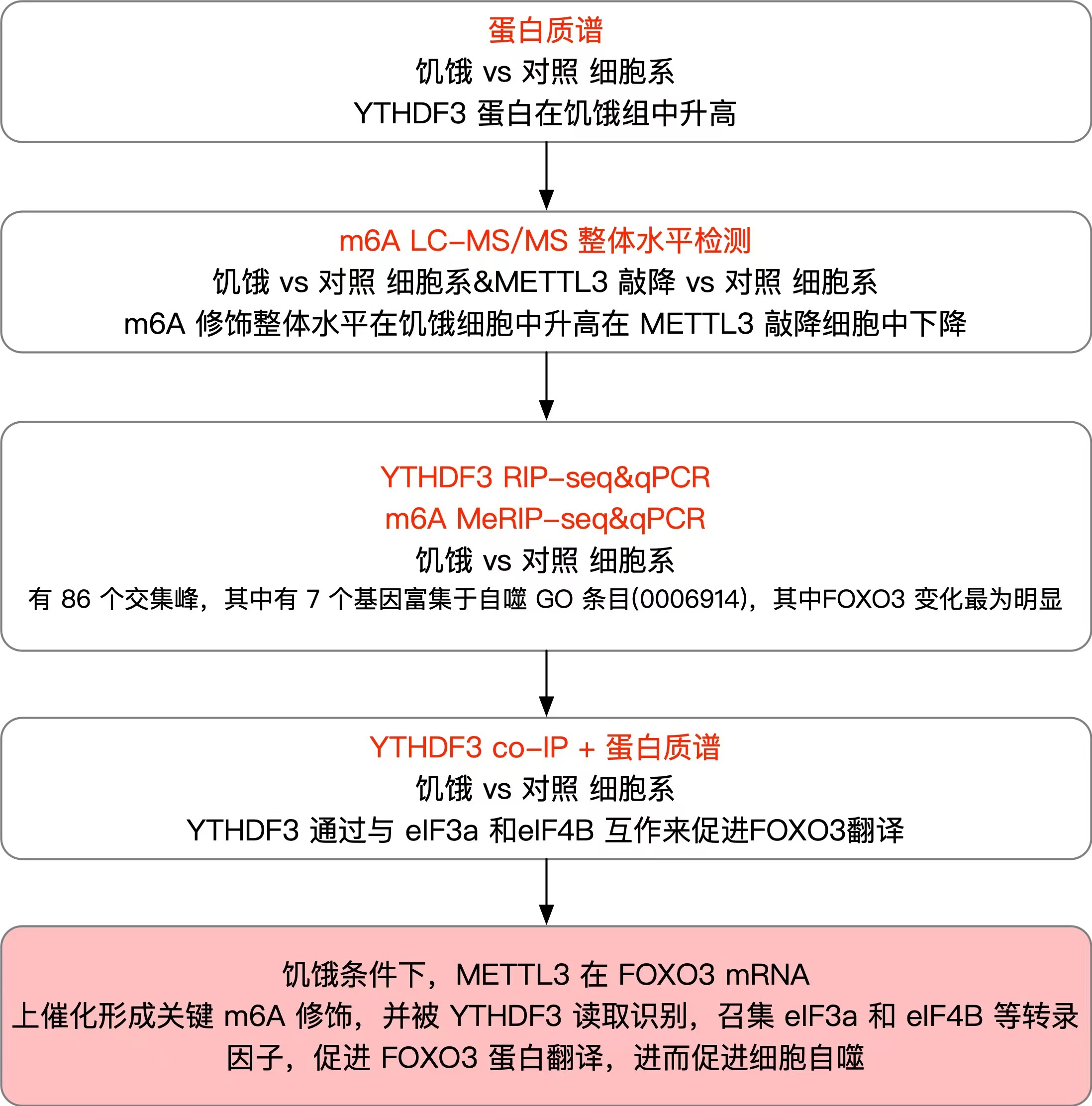
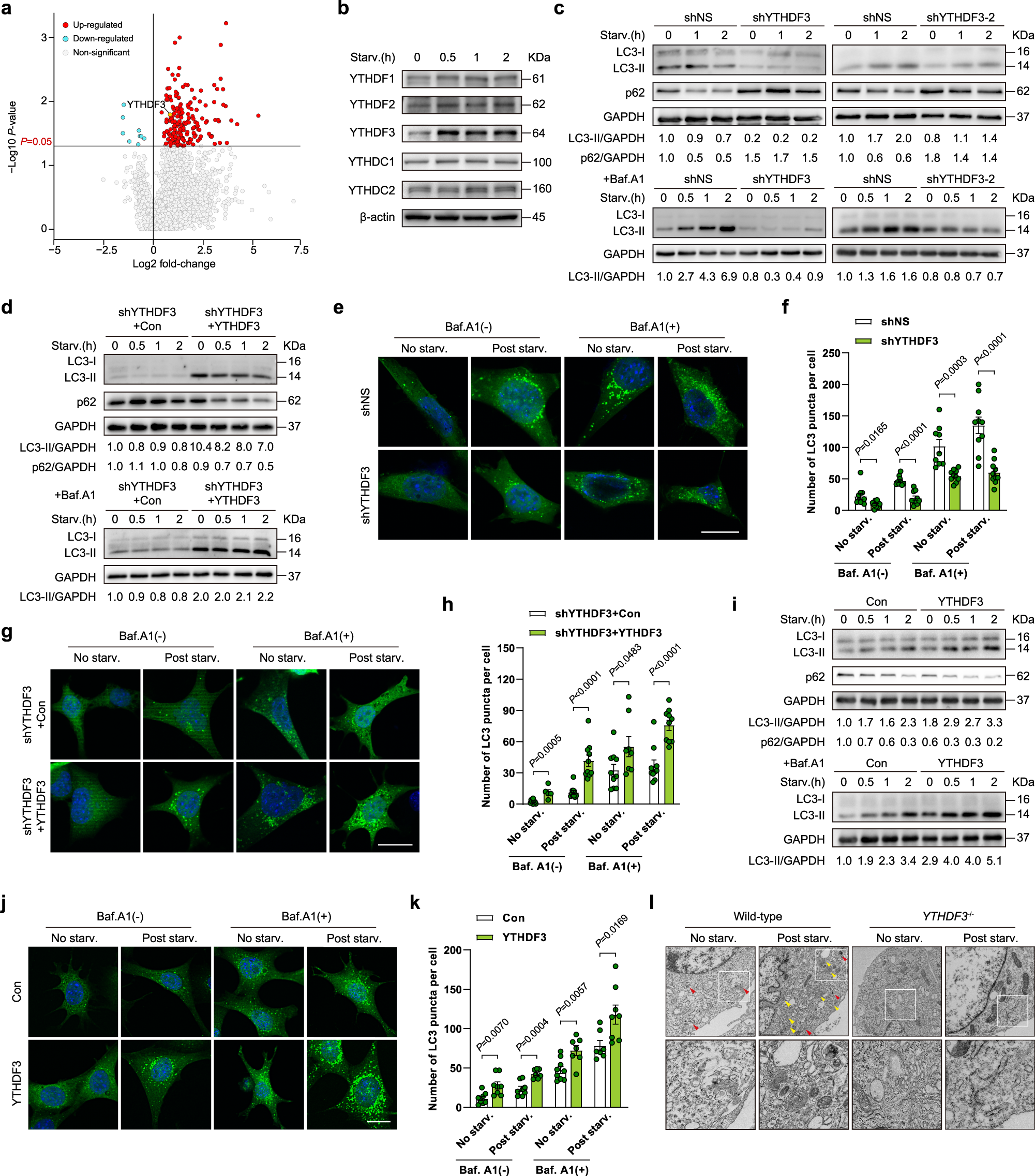
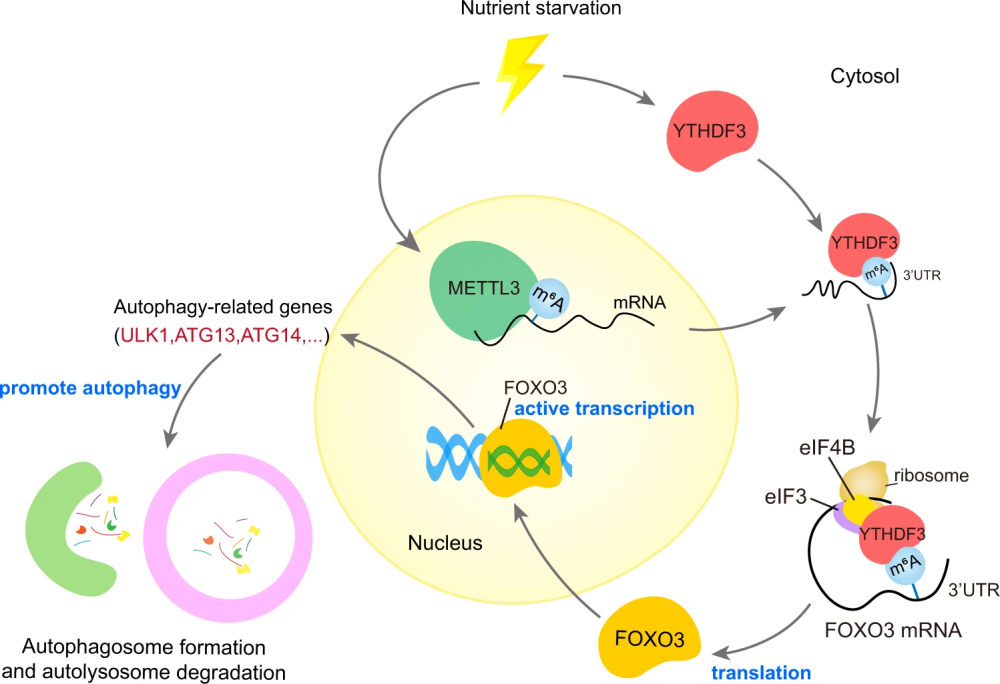
作者通过蛋白质谱实验发现,在低营养饥饿处理的小鼠胚胎成纤维细胞系当中,YTHDF3 这个 m6A Reader 蛋白的水平显著升高。为了检验 YTHDF3 对于自噬的作用,作者设计了 YTHDF3 敲降的细胞系,发现自噬标志蛋白 LC3-II 在 YTHDF3 敲降细胞系饥饿处理后下降,但自噬溶酶体中本来应该被消化的蛋白 p62 却在 YTHDF3 敲降细胞系饥饿处理后上升,说明 YTHDF3 敲降降低了自噬流(autophagy flux)现象。如果在 YTHDF3 敲降细胞中使用载体复原 YTHDF3,则 LC3-II 蛋白浓度升高,而 p62 蛋白则逐渐被消化。如果过表达 YTHDF3,则进一步升高 LC3-II、降低 p62 蛋白的水平。作者还使用 CRISPR/Cas9 系统构建了 YTHDF3 完全敲除的纯合子小鼠胚胎,荧光显微镜观察发现细胞中自噬小体和自噬溶酶体的数目明显减少。综上所述,作者认为 YTHDF3 的上调对于饥饿处理条件下的自噬诱导是不可或缺的。
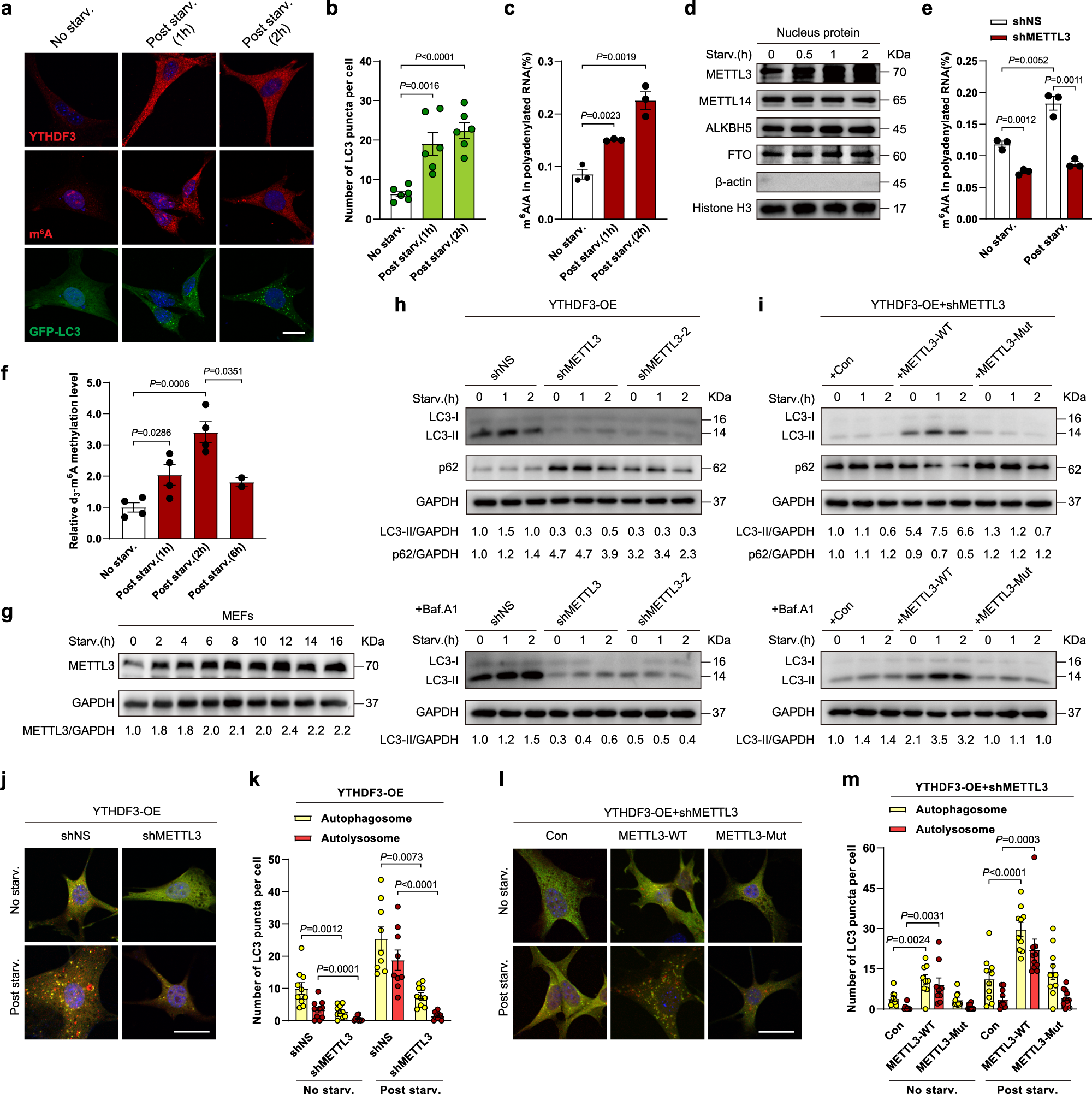
由于 YTHDF3 是一个 m6A Reader 蛋白,作者因此假设 YTHDF3 可能通过 m6A 来促进自噬作用。通过LC-MS/MS 检验 m6A 的整体水平,作者发现饥饿处理后细胞中 mRNA 的 m6A 整体水平升高。通过 Western Blot 检测 m6A 经典 Writters 和 Erasers 的蛋白质水平,作者发现饥饿处理可以显著提升 m6A Writter 蛋白 METTL3 的水平。作者于是设计 METTL3 敲降细胞系,通过LC-MS/MS 检验 m6A 的整体水平,发现 METTL3 敲降后细胞中 mRNA 的 m6A 整体水平下降。为了检测饥饿处理条件下细胞中 METTL3 蛋白的活性,作者在小鼠胚胎成纤维细胞中构建了 METTL3 FLAG 标记融合蛋白,并使用分离得到的 METTL3 FLAG 标记融合蛋白在氘(deuterium)同位素标记的 d3-SAM 作为甲基供体的体外环境下催化含有 RRACH 保守基序(motif)的 RNA 探针发生 m6A 甲基化修饰。结果显示:饥饿细胞中分离得到的 METTL3 蛋白比对照组细胞来源的 METTL3 蛋白对体外 RNA 探针实现了更高比例的 d3-m6A 修饰,说明饥饿处理可以提升 METTL3 蛋白的 m6A 修饰能力。作者因此怀疑 METTL3 介导的 m6A 修饰可能对于 YTHDF3 促进自噬作用至关重要。为了验证这一假设,作者在 YTHDF3 过表达的细胞中敲降 METTL3,结果发现饥饿诱导的 LC3-II 积累和 p62 降解现象均得到了显著的减弱。在饥饿处理的 YTHDF3 过表达细胞中,METTL3 的敲降可导致自噬小体和自噬溶酶体的减少。在此基础上,使用野生型 METTL3 基因质粒转染可以在 LC3-II 蛋白水平上提升自噬作用,但使用无催化活性的突变型 METTL3 基因质粒转染则起不到复原的效果。综上所述,YTHDF3 需要 METTL3 介导的 RNA m6A 修饰来促进自噬作用。
3、饥饿条件下,受抑制的 RPS27a-METTL3 结合关系起到了稳定 METTL3 蛋白的作用
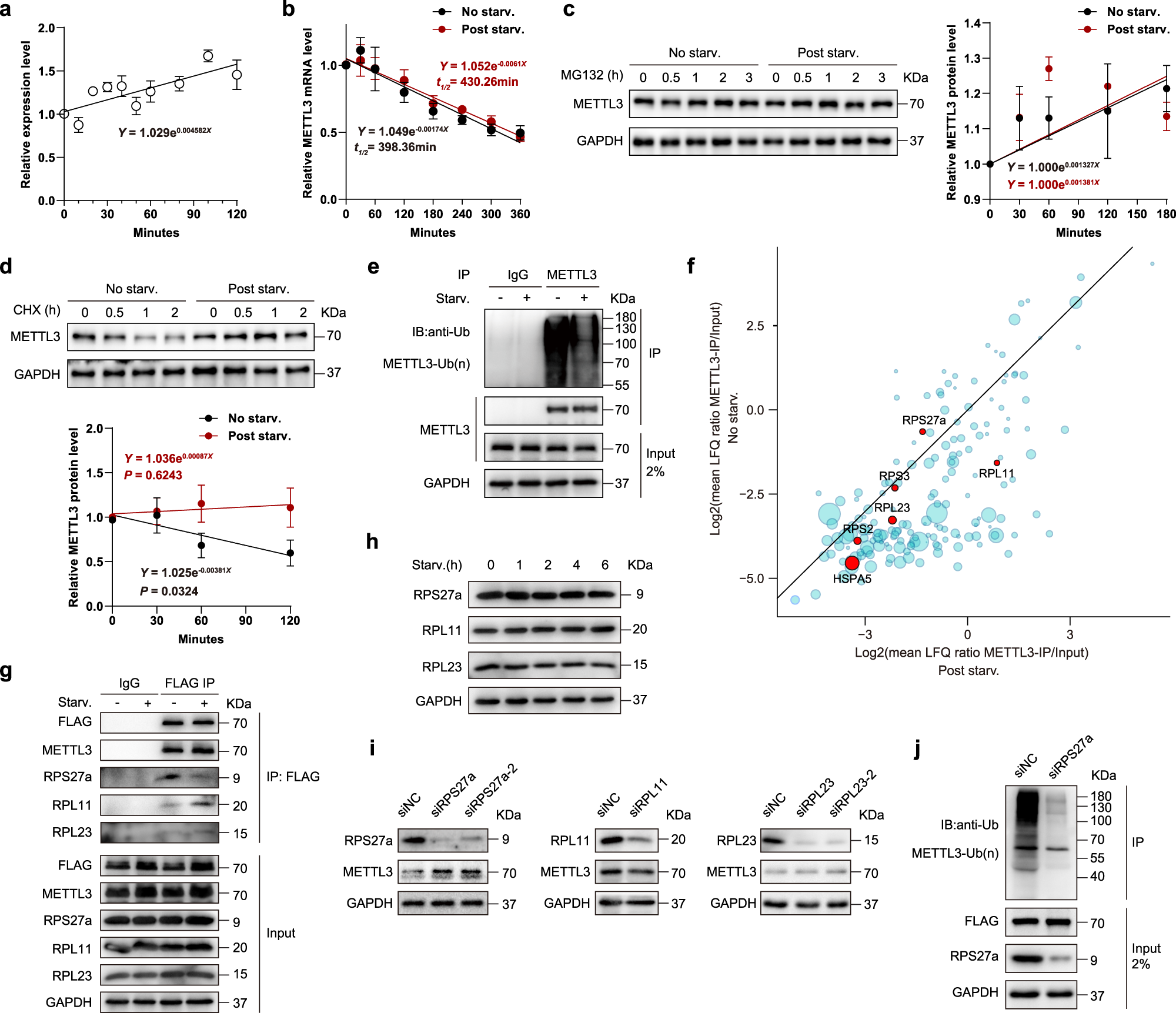
4、YTHDF3 识别 FOXO3 mRNA 上在饥饿条件下诱导产生的 m6A 修饰
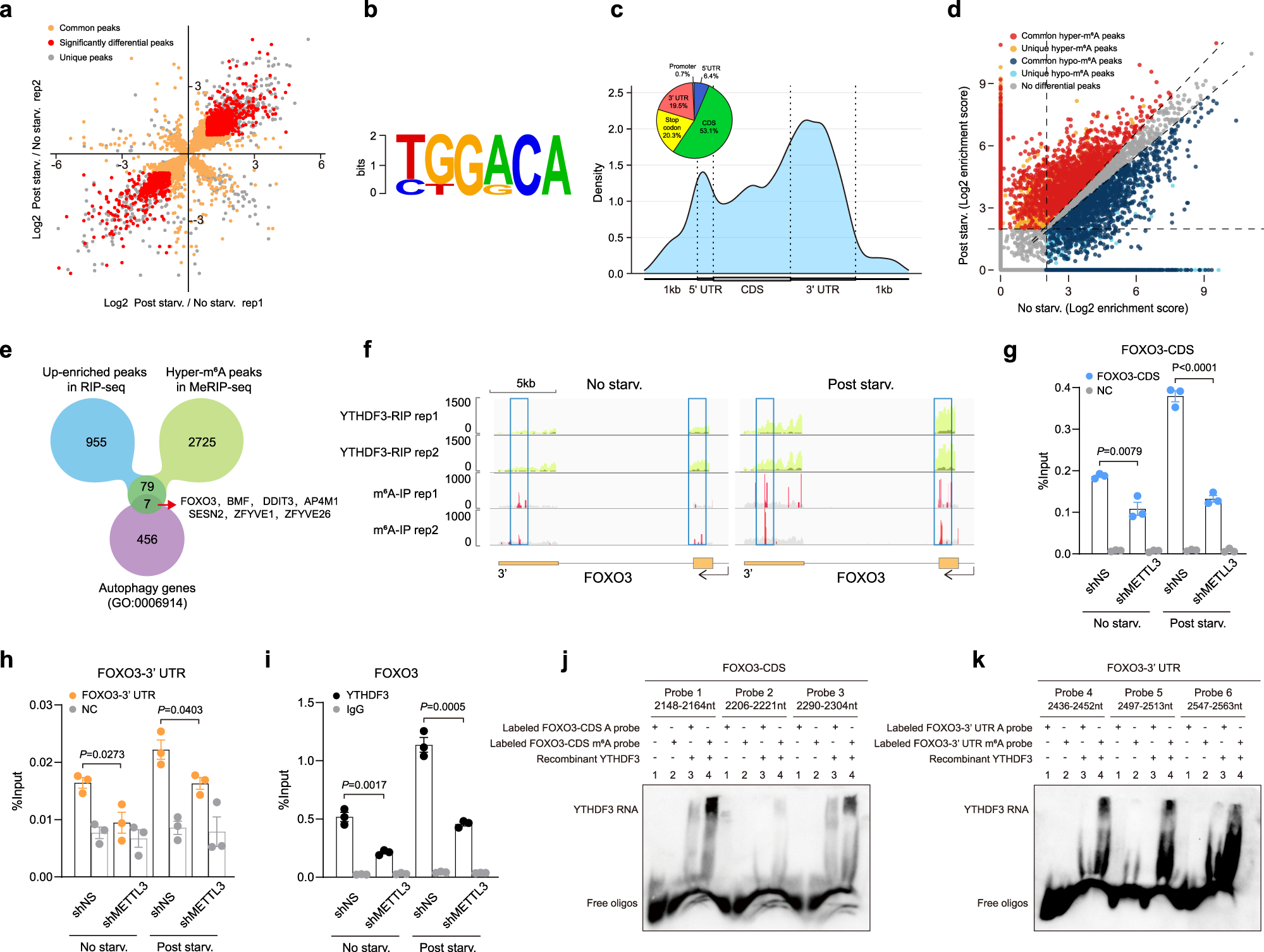
针对 YTHDF3 蛋白,作者进行了两次独立的RIP-seq 实验,在饥饿组中分别发现了 4881 和 5013 个 YTHDF3 结合峰,在对照组中分别发现了 2997 和 2865 个 YTHDF3 结合峰。通过将上述两个生物学重复中检测到的转录本取交集,作者发现了饥饿条件下 3424 个 YTHDF3 结合上调的转录本和 1814 个 YTHDF3 结合下调的转录本,其中有 1041 个 YTHDF3 显著结合上调的转录本和 535 个 YTHDF3 显著结合下调的转录本(以 fold change 绝对值 1.8 为阈值,定义“显著结合上/下调”)。YTHDF3 结合位点呈现出“GGAC”的特征 motif。这些结合点大多位于蛋白质编码区序列(CDS)和 3′UTR 当中,特别是集中于终止密码子附近。以上这些特征与以往文献中报道的 m6A 修饰峰的特征相似,因此作者认为 YTHDF3 结合的这些区域主要是发生了 m6A 修饰的区域。
作者随后对饥饿处理的细胞和对照组细胞进行了 m6A MeRIP-seq,发现了饥饿组中 2811 个峰的 m6A 甲基化程度上升,2552 个峰的 m6A 甲基化程度上升。为了寻找 YTHDF3 的 m6A 靶标,作者将 YTHDF3 RIP-seq 当中饥饿组的富集峰与 m6A MeRIP 测序当中饥饿组上调的峰取交集,得到了 86 个交集峰。其中,有 7 个基因富集到了 GO 条目 0006914 当中,也就是自噬(Autophagy)通路,它们包括了:FOXO3, BMF, DDIT3, AP4M1, SESN2, ZFYVE1, 和 ZFYVE26 这 7 个基因。通过针对 YTHDF3 的 RIP-qPCR,这 7 个基因当中的 6 个都被验证了与 YTHDF3 蛋白在饥饿处理条件下的结合,并且 FOXO3 在 RIP-qPCR 中的富集尤其明显。根据早前的文献报道,FOXO3 是一个参与自噬的重要转录因子。进一步的免疫印迹实验显示,敲降 YTHDF3 可以降低 FOXO3 和 ZFYVE1 的表达,而过表达 YTHDF3 则会起到反效果。作者额外选取了自噬相关的几个经典基因进行免疫印迹实验,但发现它们的表达都和 YTHDF3 无关。早前的文献报道显示,ZFYVE1 基因并不抑制自噬作用,因此作者将其也排除了,仅留下 FOXO3 基因进行后续的研究。YTHDF3 RIP-seq 以及 m6A MeRIP-seq 实验结果已经显示,在饥饿条件下,FOXO3 基因 mRNA 上的 m6A 修饰峰位于 CDS 和 3'UTR 当中。为了验证 YTHDF3-FOXO3 mRNA 互作依赖于 METTL3 介导的 m6A 修饰,作者在细胞系中敲降了 METTL3,m6A MeRIP-qPCR 结果显示,无论是在 FOXO3 mRNA 的 CDS 还是 3'UTR 区域,都出现了 m6A 修饰水平的下降;YTHDF3 RIP-qPCR 结果则显示,YTHDF3-FOXO3 mRNA 结合升读也下降。作者进一步设计了 YTHDF3 重组蛋白,还设计了生物素标记的带有或不带有 m6A 修饰的 FOXO3 mRNA 的 CDS 区和 3'UTR 区的多种 RNA 探针,进行 EMSA 实验。结果显示,对于 YTHDF3 重组蛋白,无论是对于 CDS 区还是 3'UTR 区,只要是带有 m6A 修饰的探针,EMSA 信号就强;只要是不带 m6A 修饰的探针,EMSA 信号就弱。其中,落在 CDS 区内的两个探针的 EMSA 信号尤其强,其覆盖范围包括了 2158nt, 2151nt, 2163nt 和 2295nt 这几个关键的腺苷酸位点,它们可能帮助 YTHDF3 识别 FOXO3 的终止密码子。总之,上述实验结果证明饥饿条件下 METTL3 介导的 m6A 高甲基化对于 YTHDF3-FOXO3 mRNA 的识别互作是必不可少的。
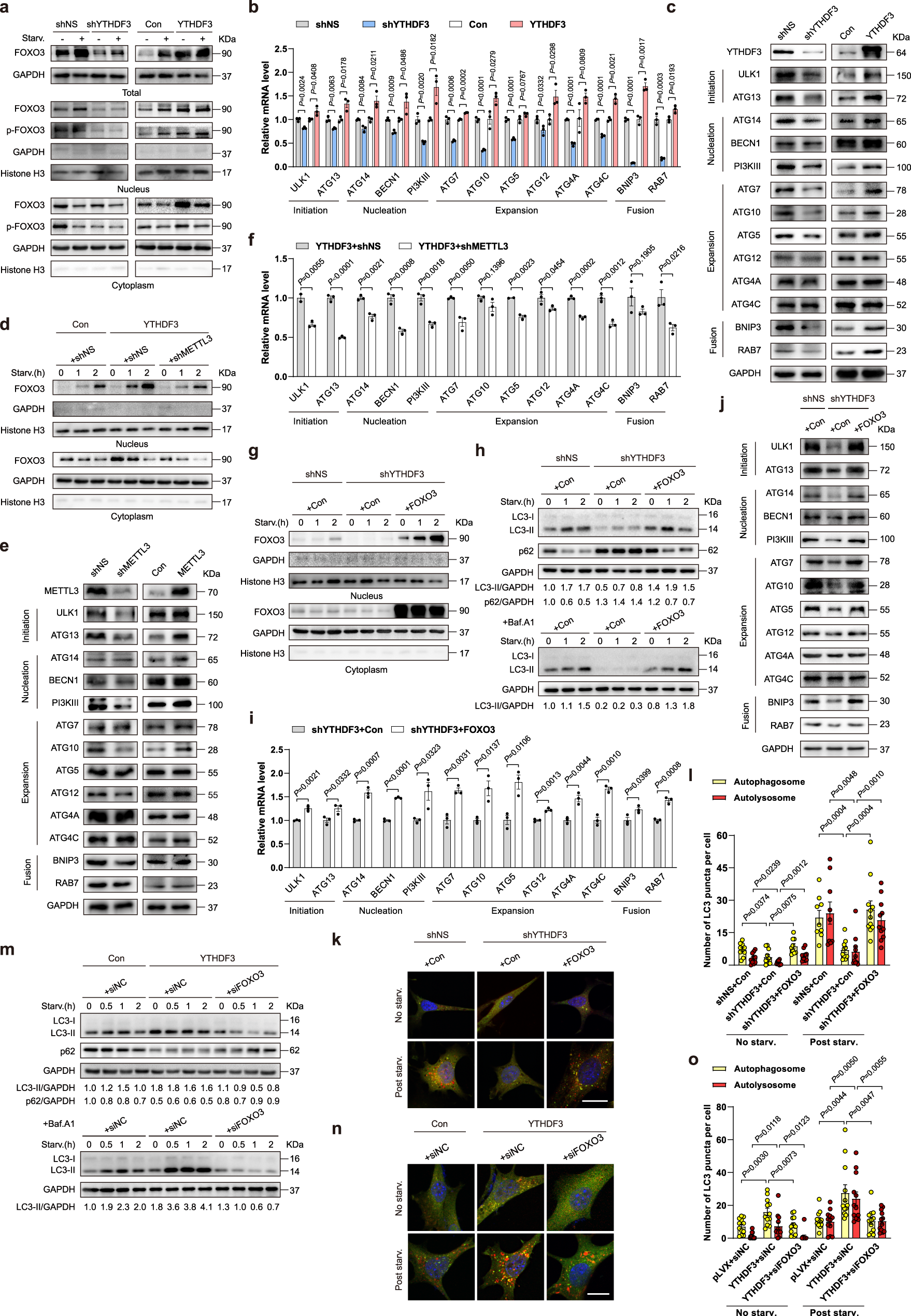
5、YTHDF3 通过 FOXO3 促进自噬
作者还在 YTHFD3 敲降细胞系中进行了 FOXO3 回补实验,发现 FOXO3 蛋白水平得以复原,并且自噬标志蛋白 LC3-II 的表达也得到复原,而自噬溶酶体中的蛋白 p62 则在 FOXO3 回补后逐渐被消化掉。类似的结果(自噬小体和自噬溶酶体的增加)也在荧光显微镜实验中发现,进一步印证了 YTHDF3 通过 FOXO3 促进自噬。
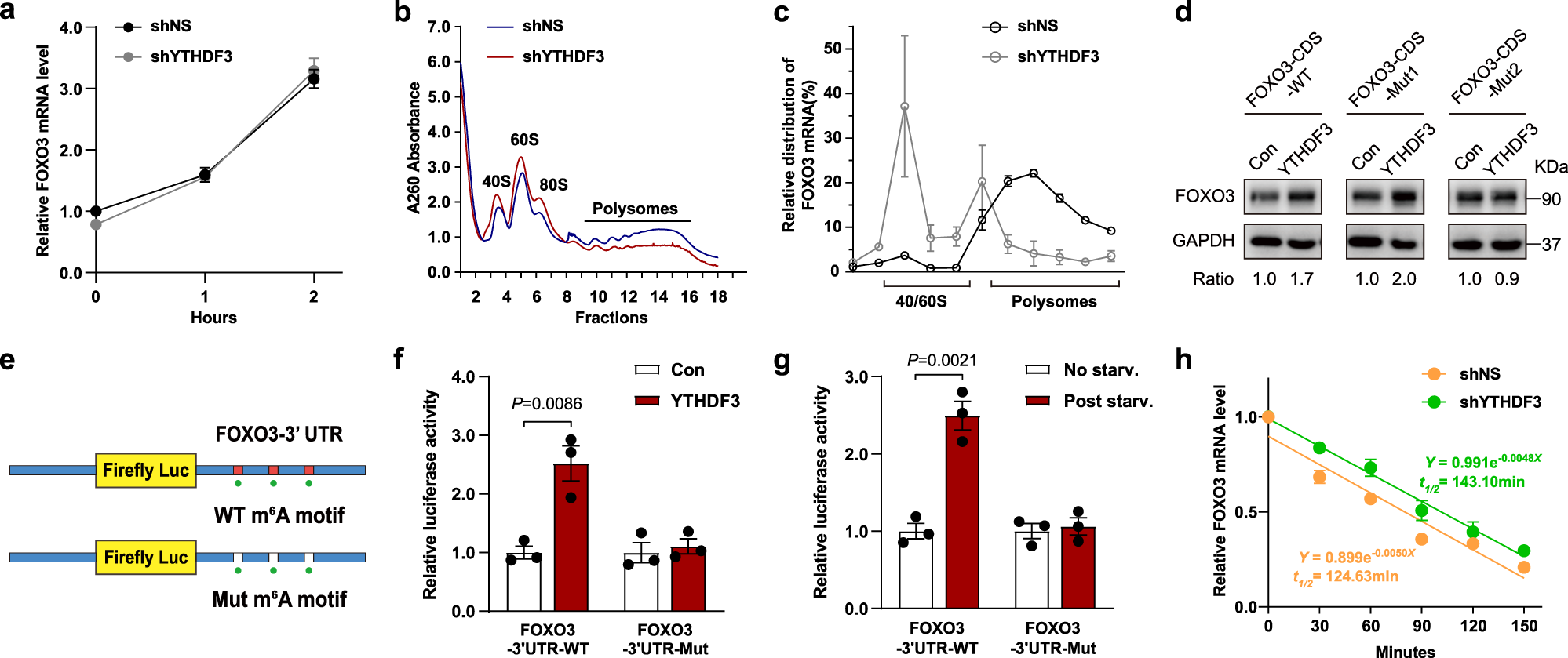
6、YTHDF3 促进 FOXO3 的翻译,但是不影响 FOXO3 mRNA 的稳定性
作者随后进行了点突变实验,来验证 FOXO3 mRNA CDS 区上 m6A 峰中的 m6A 修饰对 YTHDF3 识别的作用。作者将 FOXO3 CDS 区上最接近终止密码子的 m6A 修饰经典 motif RRACH 上的腺苷(A)突变为了胸苷(T),发现对于突变型的 FOXO3 mRNA 而言,YTHDF3 不能再起到促进 FOXO3 翻译的作用。这说明 FOXO3 CDS 区上的最接近终止密码子的 m6A 修饰是 YTHDF3 的识别对象。作者也针对 FOXO3 mRNA 上 3'UTR 上的 m6A 修饰做了类似的点突变工作,并通过荧光素酶报告实验验证了 3'UTR 上的 m6A 修饰与 YTHDF3 的互作。
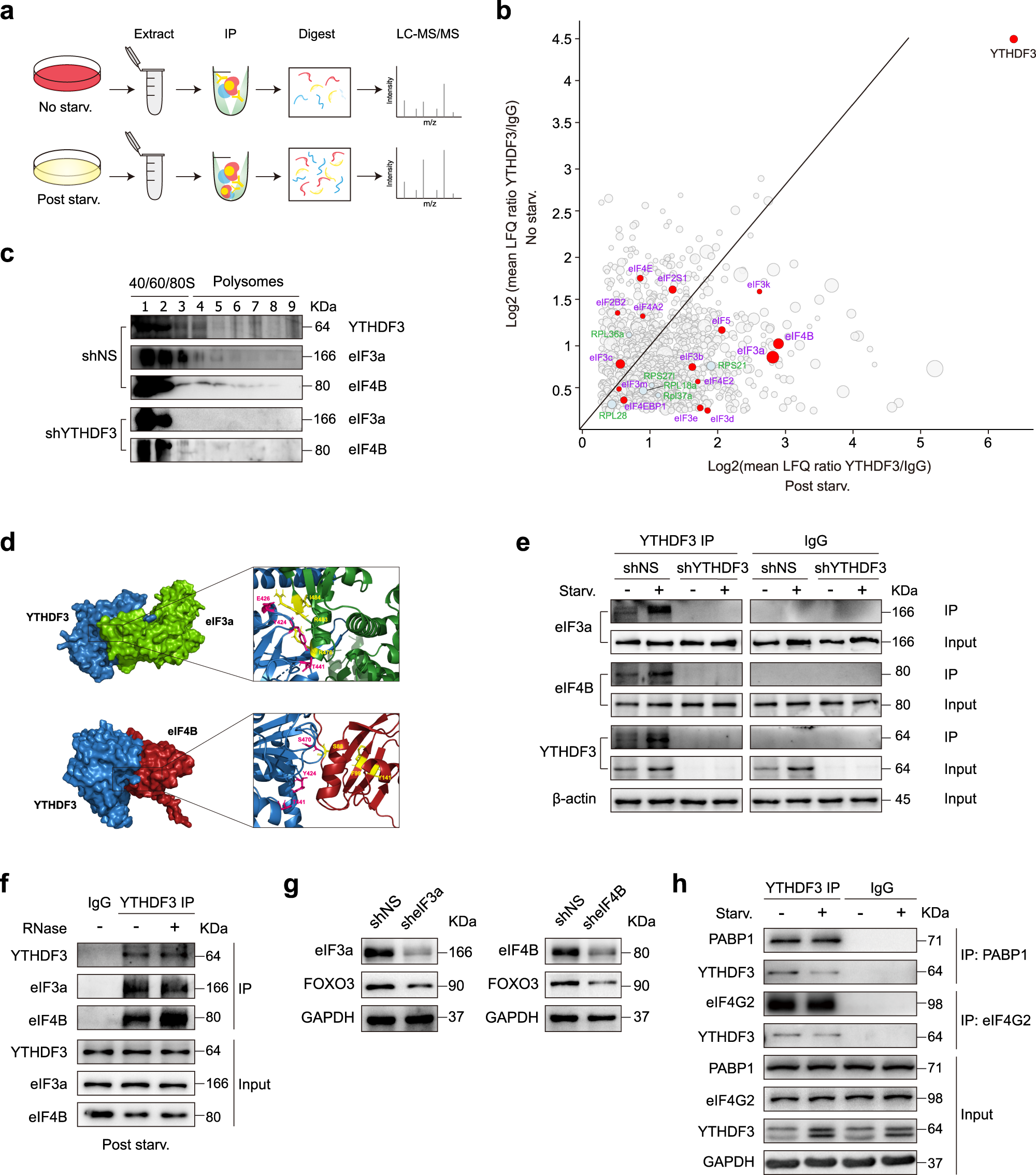
7、YTHDF3 通过与 eIF3a 和 eIF4B 互作来促进 FOXO3 翻译
云序生物m6A修饰研究五大模块
m6A RNA修饰测序(m6A-meRIP-seq)
对m6A RNA甲基化,目前流行的检测手段为m6A-MeRIP-Seq技术,适用于m6A RNA甲基化谱研究,快速筛选m6A RNA甲基化靶基因。云序可提供mRNA和多种非编码RNA的m6A测序:
- m6A 全转录组测序(涵盖mRNA,LncRNA,circRNA)
- m6A LncRNA测序(涵盖LncRNA和mRNA)
- m6A Pri-miRNA测序(涵盖Pri-miRNA和mRNA)
- m6A mRNA测序
- m6A miRNA测序
LC-MS/MS检测整体RNA修饰水平
精准高效,可以实现一次检测,9类修饰水平检测,一步到位。
比色法检测整体RNA修饰水平
快速检测m6A整体甲基化水平
03 m6A RNA修饰上游酶的筛选
m6A RNA修饰相关酶PCR芯片
寻找上游直接调控m6A RNA甲基化的甲基转移酶。
04 m6A RNA修饰靶基因验证
MeRIP-qPCR/GenSeq® MeRIP试剂盒
云序提供各类不同修饰的meRIP-qPCR服务以及销售GenSeq® MeRIP试剂盒,可针对mRNA,lncRNA,环状RNA等不同类型的RNA分子进行检测,低通量验证RNA修饰靶基因表达水平。
05 机制互作研究
5.1 RIP-seq/qPCR/GenSeq® RIP试剂盒
筛选或验证RNA修饰直接靶点,研究RNA修饰靶基因的调控机制。
5.2 RNA pull down -MS/WB
筛选或验证目标RNA互作基因或蛋白,研究相应的分子调控机制。
5.3 双荧光素酶实验
验证两基因互作,研究相应的分子调控机制。
5.4 ChIP-seq
筛选或验证目标蛋白与DNA互作,研究相应的分子调控机制。
云序生物服务优势
优势二:累计完成数千例 RNA甲基化测序样本,全面覆盖医口、农口等各类样本。
优势三:全面检测mRNA和各类非编码RNA(circRNA,lncRNA,Pri-miRNA等)。
优势四:提供m6A一站式服务:m6A整体水平检测、m6A测序、MeRIP-qPCR验证、RIP和RNA pull-down等。
优势五:率先研发超微量MeRIP测序技术,RNA量低至500ng起。
优势六:国内较全的RNA修饰测序平台,提供m6A、m5C、m1A、m7G、m3C、O8G、ac4C乙酰化和2'-O-甲基化测序。
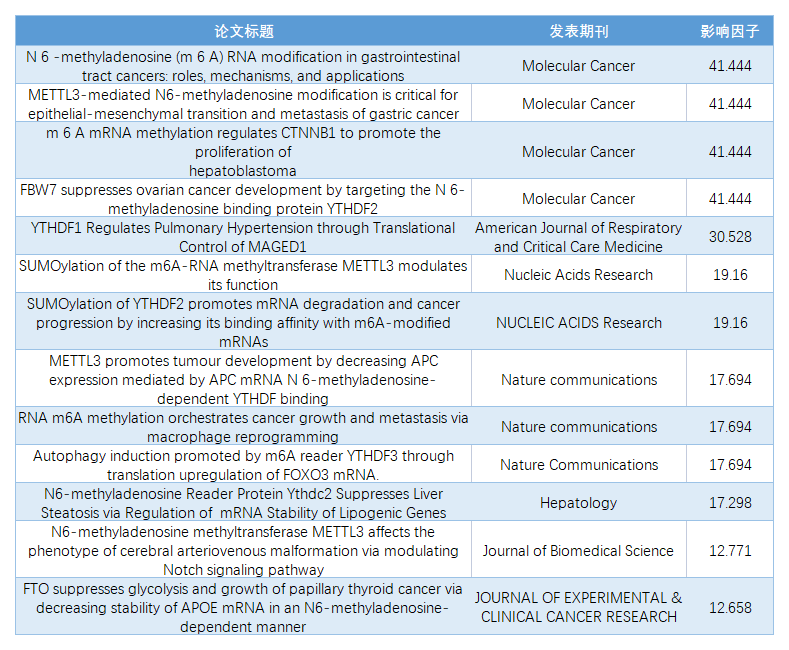
云序客户 RNA m6A 修饰高分文章列表
相关产品
往期回顾
客户文章1区IF 12+ |m6A甲基化测序助力FTO抑制PTC糖酵解代谢机制研究
客户文章|m6A甲基化测序助力脓毒症诱导的ARDS表位机制研究
1区,IF=27|借力m6A甲基化修饰,探索肾细胞癌耐药性机制研究
1区,IF=27| 云序m6A MeRIP-seq助力鳞状细胞癌机制研究!
时间不够?云序m6A甲基化测序技术助力用户3-5个月发表5分文章!
超详细图文版:如何实现m6A测序数据可视化?
云序用户 1区,IF=23.168 | 多组学联合分析揭示胰腺癌中 RNA 乙酰化修饰的重要靶点
1区,IF=19.16| 云序RNA乙酰化测序acRIP-seq助力病毒复制机制研究!
客户文章|新型RNA修饰之m7G揭示急性髓系白血病发病机制
1区,IF=16.8| 云序RNA乙酰化测序/acRIP-seq助力心梗机制研究!

地址: 松江区莘砖公路518号18号2楼
网址: http://www.cloud-seq.com.cn
电话: 021-64878766
邮箱: market@cloud-seq.com.cn




