1区,IF=27| 云序m6A MeRIP-seq助力鳞状细胞癌机制研究!
发布时间:2022-05-05 14:59 | 点击次数:
头颈部鳞状细胞癌(HNSCC)严重破坏咀嚼、呼吸、吞咽等基本生理功能,甚至可能危及生命。因此探讨影响HNSCC肿瘤发生和发展的因素是当前迫切需要解决的问题。m6A修饰的研究为转录后调控开辟了新的视角。然而,m6A的修饰状态及其如何参与HNSCC的进展仍不清楚。2022年4月9日云序客户上海交通大学附属第九人民医院张志愿院士课题组马海龙研究员在Molecular Cancer杂志(IF=27)上发表了文章“The m6A demethylase ALKBH5 promotes tumor progression by inhibiting RIG-I expression and interferon alpha production through the IKKε/TBK1/IRF3 pathway in head and neck squamous cell carcinoma”,发现了ALKBH5通过IKKε/TBK1/IRF3通路抑制RIG-I表达和干扰素α的产生进而促进肿瘤发生。云序生物有幸参与了该项工作中的m6A MeRIP-seq、RNA-seq以及MeRIP-qPCR验证服务。下面我们为大家介绍这篇文章的研究思路。
近期云序活动,详情点击
庆云序MeRIP-seq文章超65篇,MeRIP-seq满五送 一 (cloud-seq.com.cn)
2022云序春季在线讲座火热进行中!点击进行报名!



影响因子:27.401
发表时间:2022年4月9日
研究方法:m6A MeRIP-seq、RNA-seq、MeRIP-qPCR、RIP-qPCR
文章链接:The m6A demethylase ALKBH5 promotes tumor progression by inhibiting RIG-I expression and interferon alpha production through the IKKε/TBK1/IRF3 pathway in head and neck squamous cell carcinoma
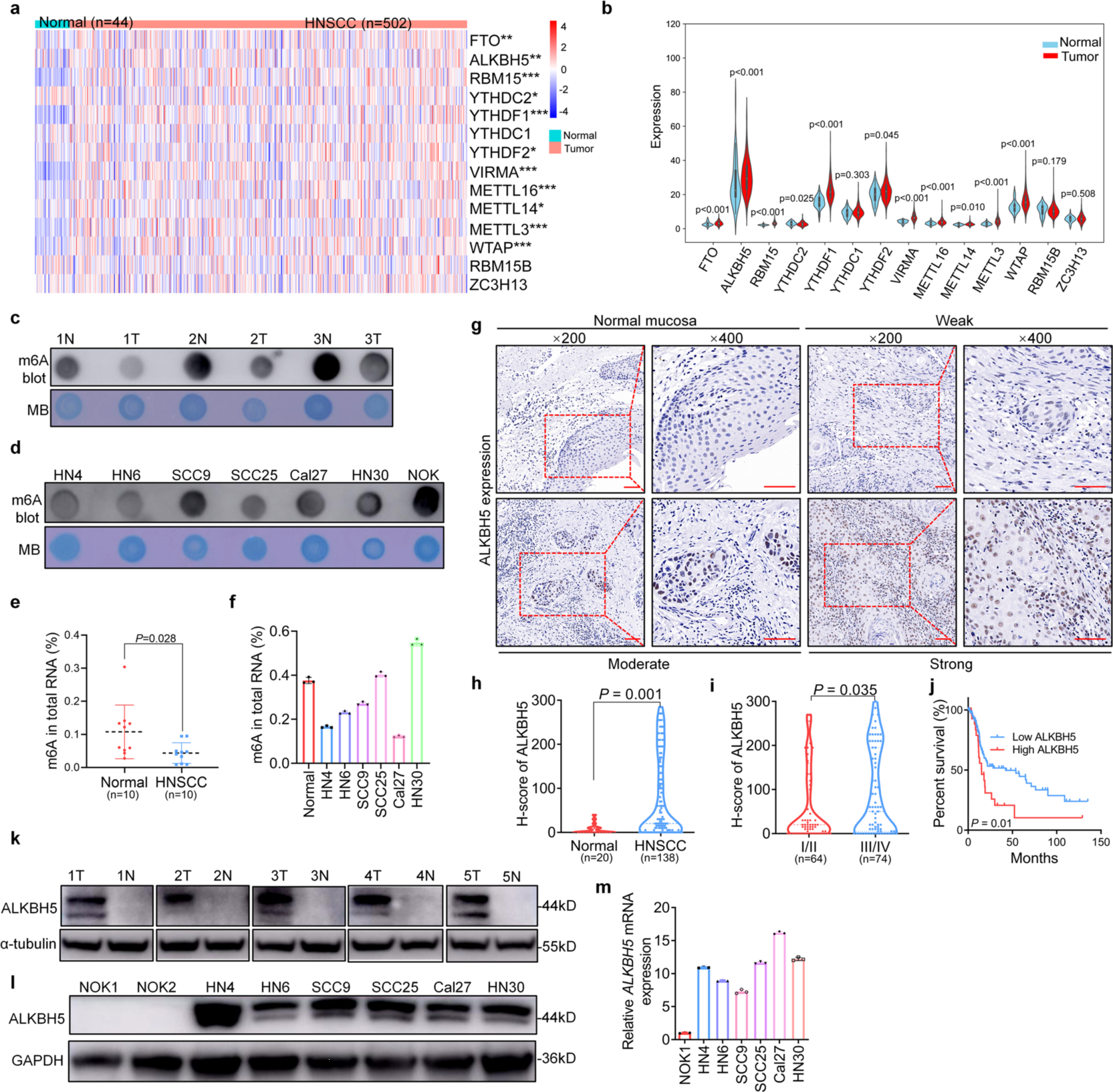
通过TCGA数据库分析了m6A writers, erasers, and readers (WERs)在HNSCC中的表达,发现AKLBH5在14个WERs中上调最显著,是HNSCC中理想的研究对象。此外, HNSCC组与配对正常组织相比m6A修饰百分比下降,大多数HNSCC细胞系的m6A修饰水平低于初级口腔角质形成细胞。因此作者推测HNSCC中m6A的下调可能与去甲基化酶的过表达有关。使用免疫组化技术进一步检测发现ALKBH5和FTO在HNSCC组织中表达上调,其高表达与HNSCC中TNM晚期和预后不良相关。根据ROC曲线,ALKBH5诊断HNSCC的敏感性为65.7%。5个肿瘤组织中ALKBH5蛋白的表达高于邻近正常口腔上皮组织。这些结果表明,在HNSCC中,m6A去甲基化酶的表达上调可促进低m6A状态,并与不良预后相关。
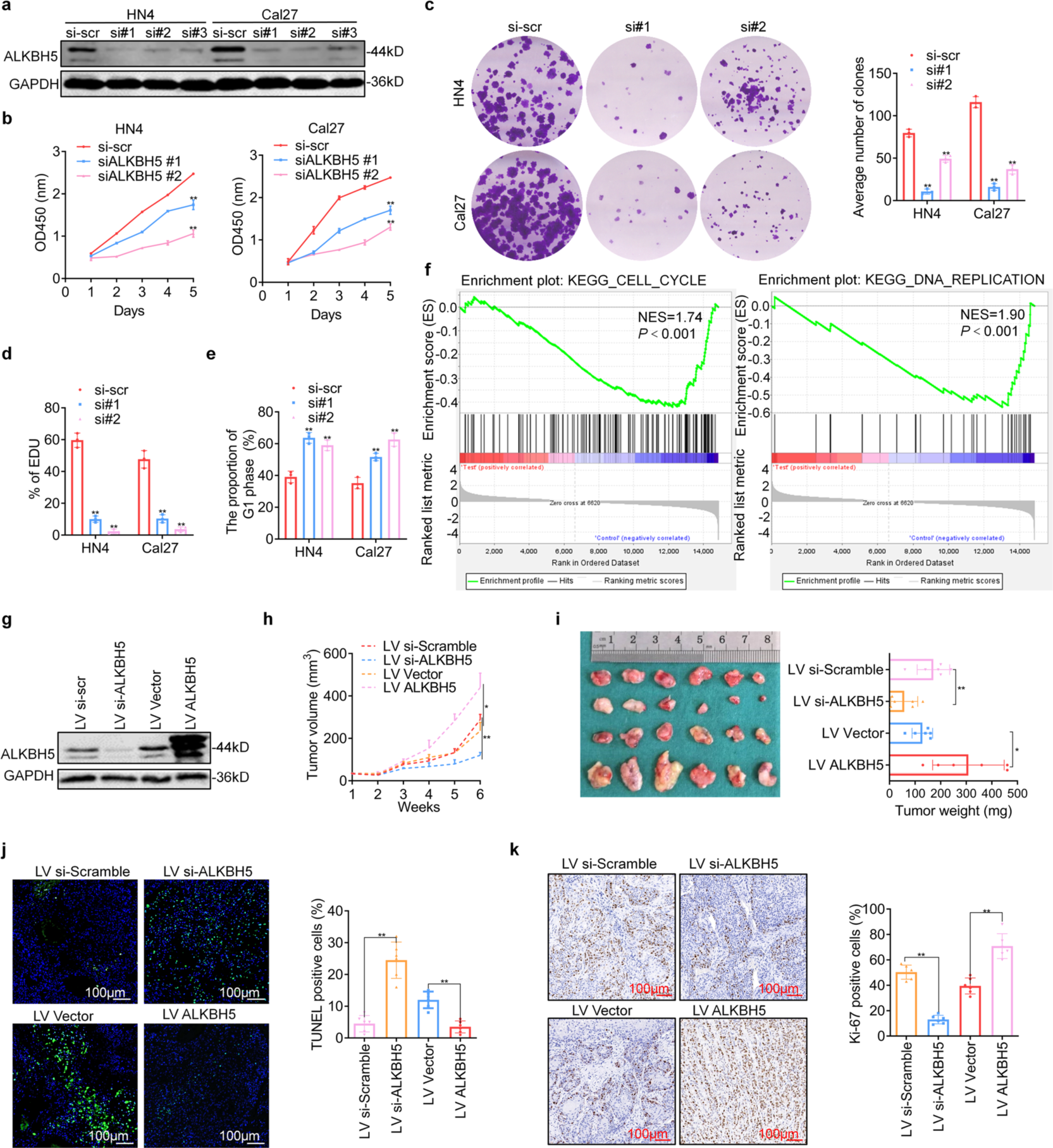
2、抑制ALKBH5可降低体外细胞增殖和体内肿瘤生长
为了探索ALKBH5在肿瘤发展中的作用,在HN4和Cal27细胞中敲低ALKBH5 ,发现显著降低了细胞增殖和克隆形成。此外,沉默ALKBH5可降低DNA复制活性,且G1期和凋亡细胞的比例也明显增加。基因集富集分析显示这些表达变化的基因与细胞周期和DNA复制过程有关。这些结果表明,ALKBH5是一个驱动HNSCC发展的致癌基因。为了进一步确定ALKBH5在肿瘤生长中的作用,在Cal27细胞系中构建了敲低和过表达模型。敲低ALKBH5可以抑制肿瘤生长,而过表达则促进肿瘤生长。此外,TUNEL染色显示,敲低ALKBH5的表达增加了细胞凋亡,而过表达则降低了细胞凋亡。以上结果表明,ALKBH5在HNSCC的发展中起着非常重要的作用。
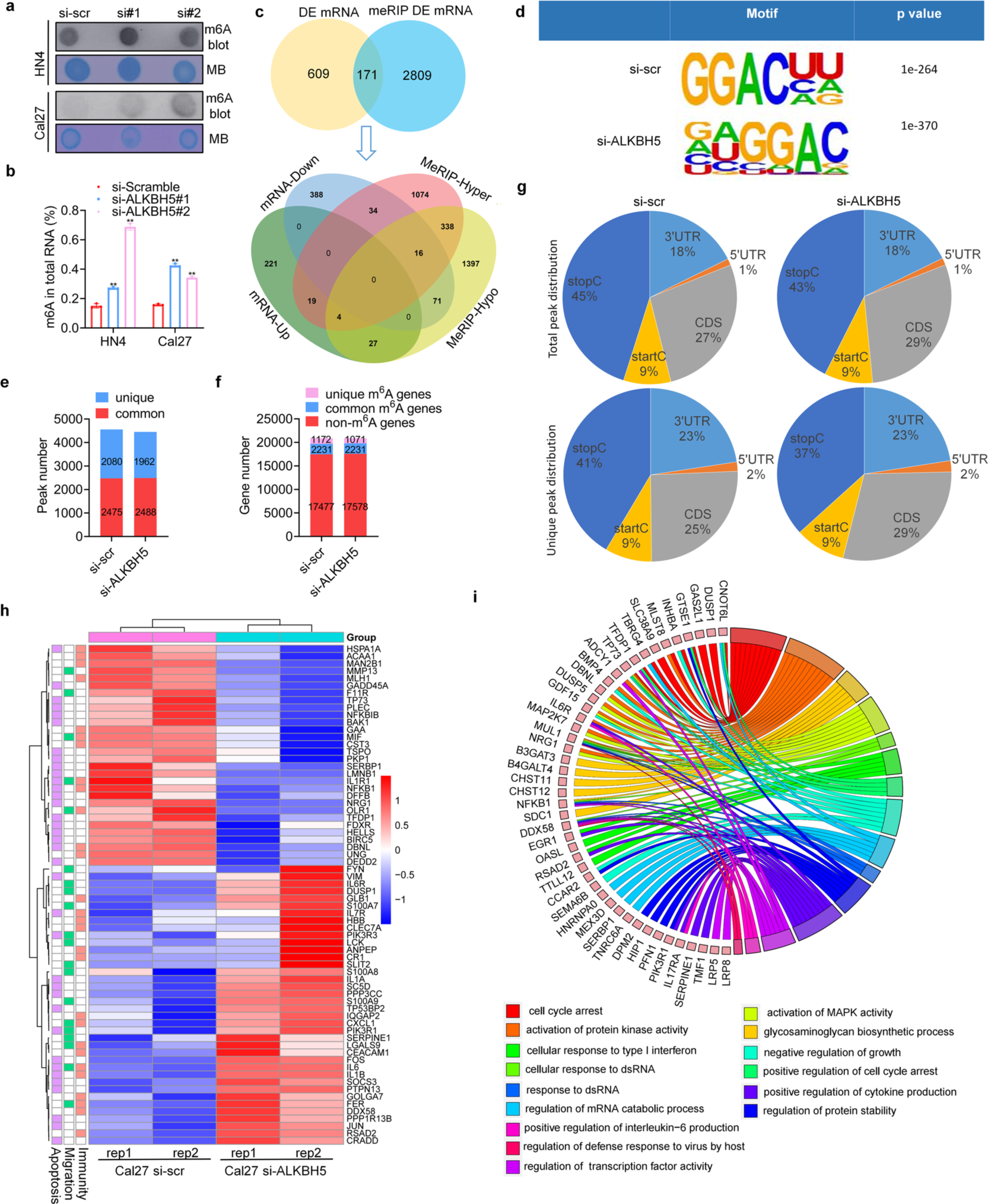
3、HNSCC中m6A修饰特征及ALKBH5下游靶点分析
接下来探究ALKBH5促进肿瘤发生的分子机制。首先m6A整体水平检测发现在HNSCC细胞系中,ALKBH5的缺失增加了m6A的总丰度。然后通过m6A MeRIP-seq和RNA-seq,共筛选出171个差异表达和m6A修饰差异基因。motif分析显示,GGACU基序在m6A位点高度富集,与m6A序列RACH一致。总体而言,对照组和ALKBH5缺陷细胞分别鉴定出2080和1962个独有的m6A峰,以及1172和1071个独有的m6A修饰基因。作者进一步研究了m6A的分布模式,在对照组和ALKBH5缺陷细胞中,总m6A峰和两组共有m6A峰分布模式相似。有趣的是,CDS区中m6A的相对增加是以一种依赖于ALKBH5的方式。为了探究ALKBH5沉默后下游的生物学过程,对差异表达基因(DEGs)进行功能富集分析。利用聚类分析方法将DEGs分为凋亡、迁移和免疫三个部分进行分析和分组。GO功能分析显示,DEGs与肿瘤发展过程,如生长的负调控和细胞周期阻滞,以及固有免疫过程,如细胞对I型干扰素和dsRNA的反应相关。
4、ALKBH5通过m6A修饰调控RIG-1的表达
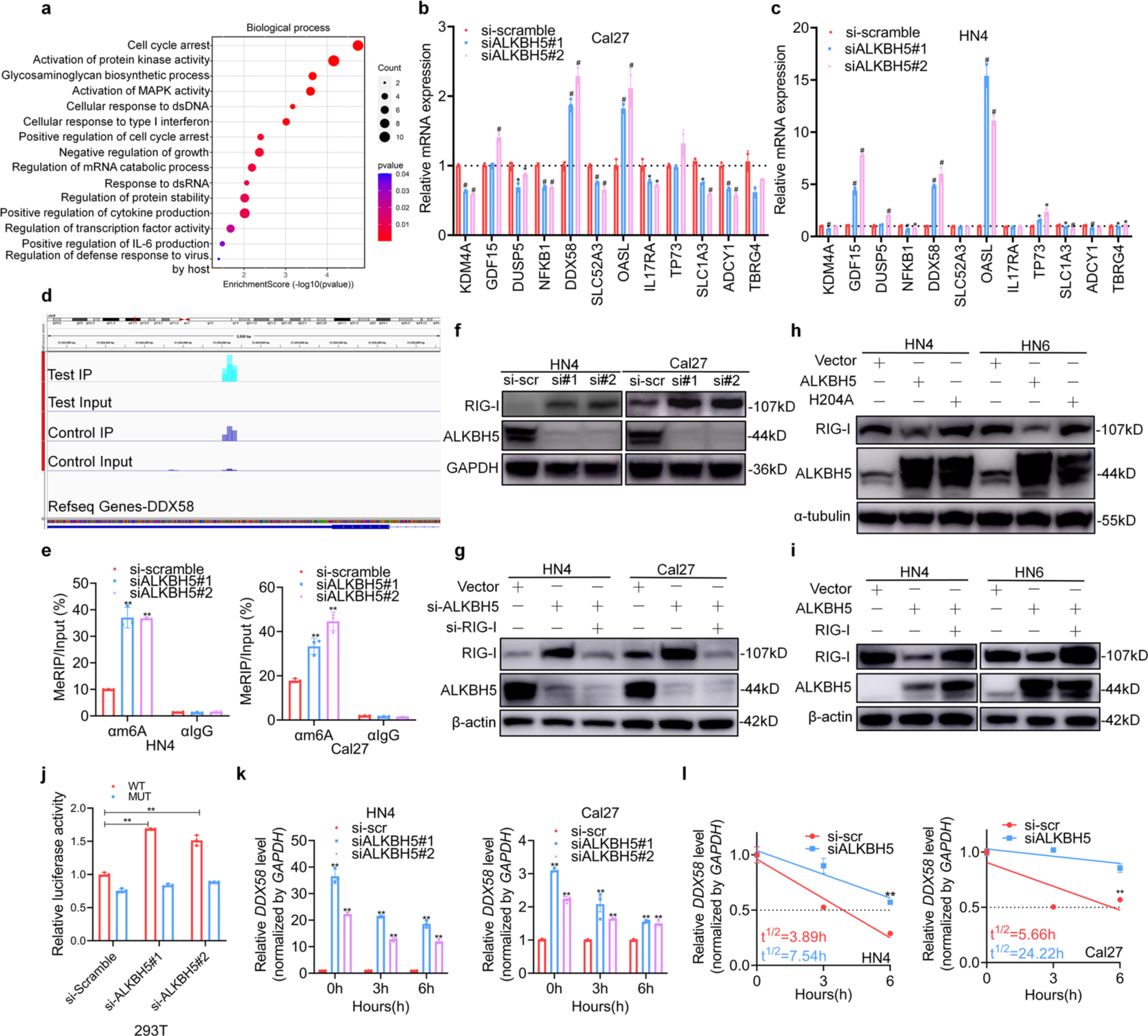
接下来通过qPCR验证DEGs的表达,包括参与细胞对I型干扰素反应的DEGs。ALKBH5敲除后,DDX58的增加最为显著,且在细胞系之间相对一致。火山图显示,与对照相比,DDX58的mRNA表达和m6A修饰水平相对较高。可视化分析显示,在DDX58 mRNA的3'UTR区,m6A显著富集。且MeRIP-qPCR实验证实,在HN4和Cal27细胞系中,ALKBH5敲除后,DDX58 mRNA的m6A修饰显著升高。这些结果表明,DDX58是HNSCC中ALKBH5介导的m6A甲基化修饰靶点。
DDX58编码RIG-I蛋白,RIG-I蛋白是一种识别病毒RNA的细胞质受体,在先天免疫和I型干扰素的产生中起着关键作用。敲除ALKBH5显著增加了RIG-I蛋白表达,说明ALKBH5通过去甲基化活性影响RIG-I的表达。同样,过表达RIG-I可逆转ALKBH5介导的抑制。此外,ALKBH5过表达抑制RIG-I介导的IFNα分泌。为了确定依赖于ALKBH5的m6A调控对RIG-I表达的影响,将m6A共识序列中的两个A突变为C, ALKBH5缺失显著提高了WT型DDX58的荧光素酶活性,而非突变型。并且通过RNA稳定性实验发现,在HNSCC细胞中,敲低ALKBH5可提高DDX58的表达,延长DDX58 mRNA转录本的半衰期。这些结果表明,ALKBH5介导的DDX58 mRNA m6A水平降低可抑制RIG-I的表达。
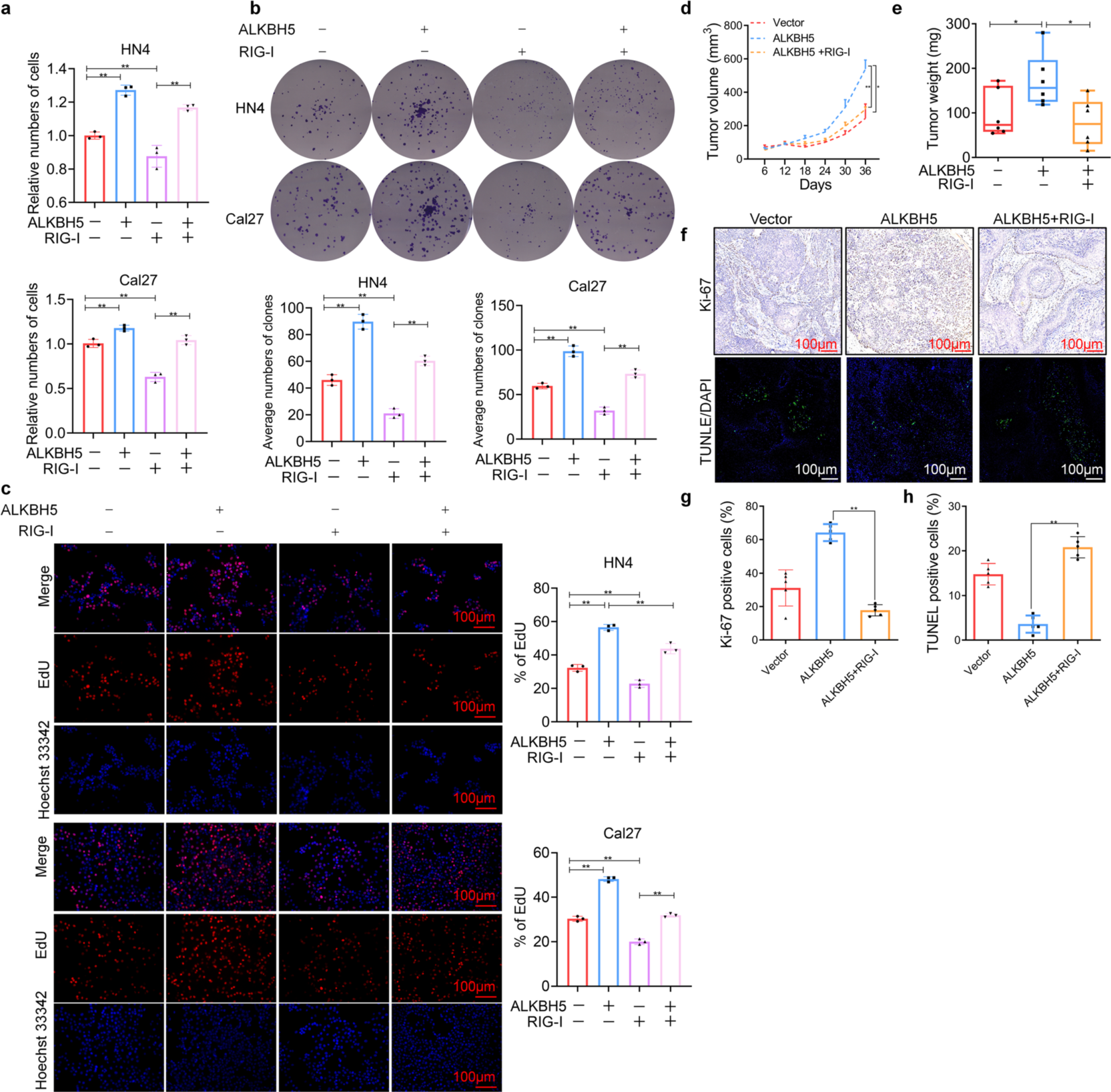
5、RIG-1的过表达逆转了ALKBH5的致癌基因作用
由于RIG-I是ALKBH5的一个新的下游靶点,因此有必要研究RIG-I在ALKBH5致癌基因中的作用。正如预期的那样,RIG-I的过表达逆转了HN4和Cal27细胞中ALKBH5过表达引起的细胞增殖和细胞群数量的增加。此外,EdU检测显示RIG-I可以降低ALKBH5介导的DNA复制活性。为了进一步支持体外实验结果,作者还制作了小鼠模型。发现过表达ALKBH5增加了肿瘤的大小和重量,并被RIG-I的表达所抑制。此外,回补RIG-I表达可缓解ALKBH5过表达引起的Ki-67指数的升高和TUNEL阳性百分率的降低。这些结果表明,抑制RIG-1表达是HNSCC中ALKBH5介导的肿瘤发生的关键事件。
6、HNRNPC是DDX58 mRNA m6A修饰的“reader”蛋白
为了找到DDX58的“reader”蛋白,并确定DDX58调控的m6A依赖机制,进行了ChIRP-MS实验。共鉴定出109个蛋白,从7个异质性核核糖核蛋白C (HNRNPC)多肽中鉴定出6个独特的多肽,它们具有最高的特异性。此外,western blot分析显示,在ALKBH5沉默后,DDX58探针显著与HNRNPC结合,并增加m6A水平。RIP-qPCR实验显示,HNRNPC抗体与RIG-I结合显著增加了RIG-I的表达。敲除RIG-I后逆转了HNRNPC过表达介导的作用,相反,敲除HNRNPC也会抑制RIG-I的表达。这些结果表明,沉默ALKBH5增加了DDX58 mRNA的m6A修饰以及随后与HNRNPC的结合,促进了DDX58 mRNA的成熟,增强了RIG-I蛋白的表达。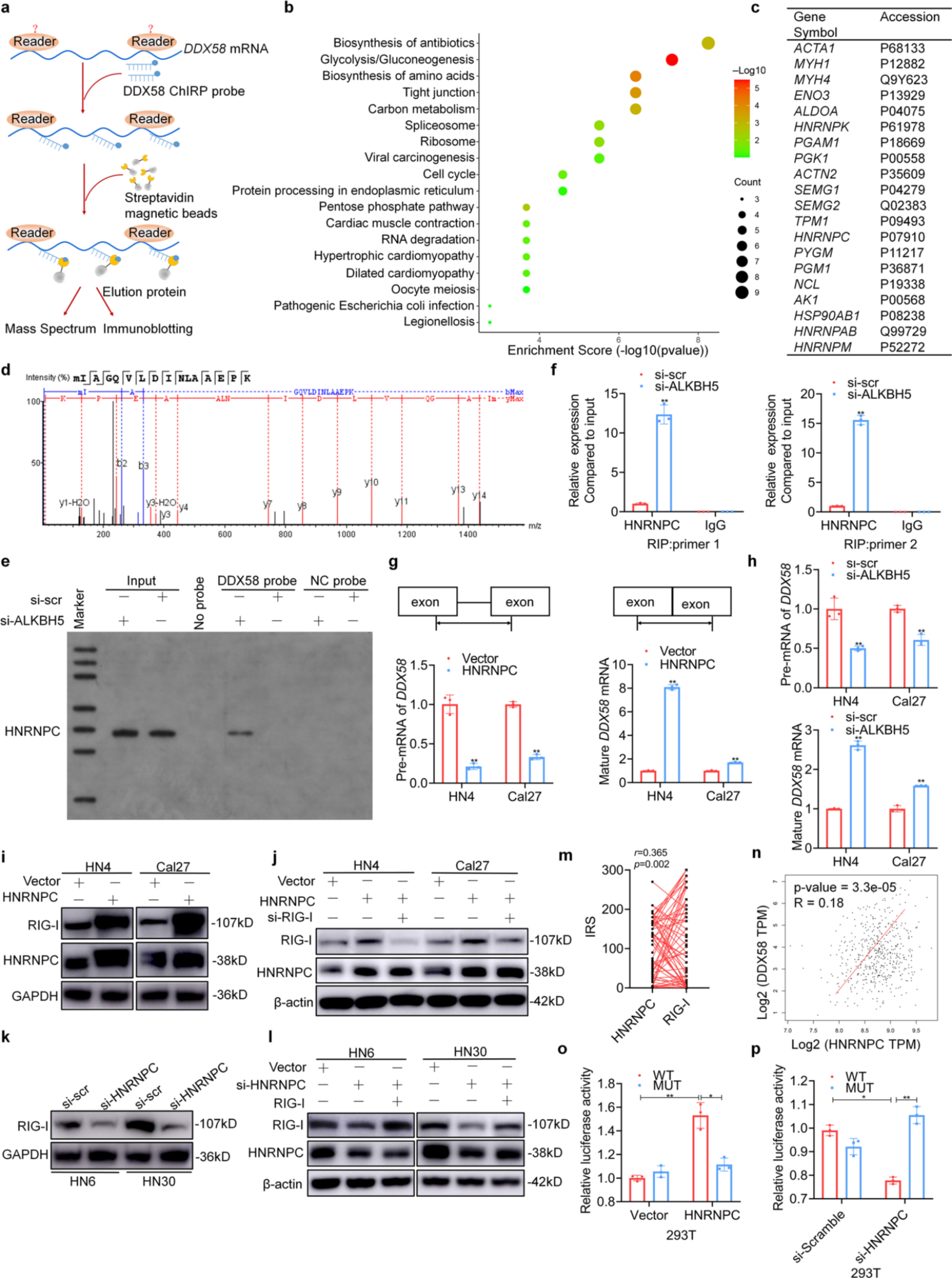
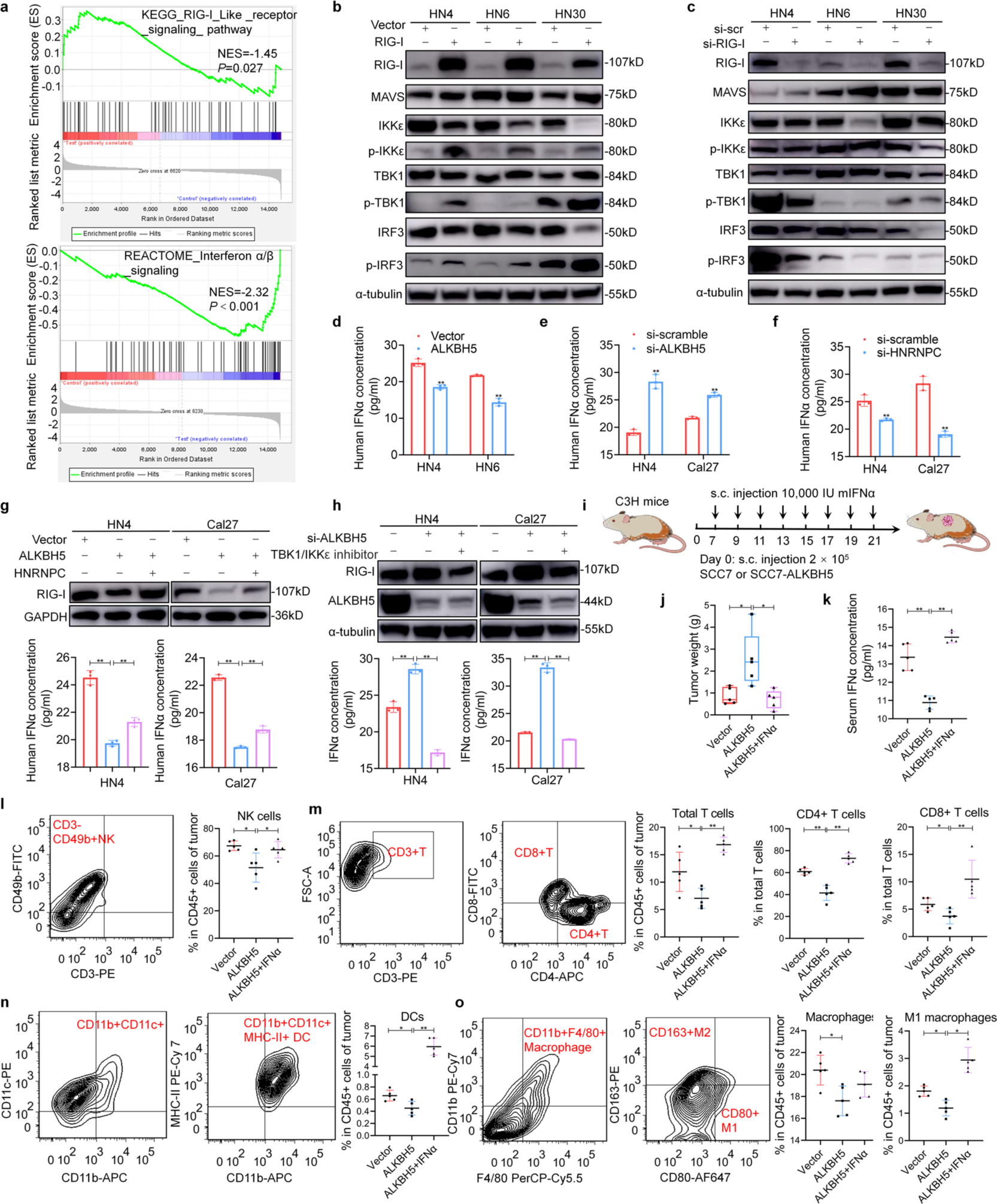
7、由ALKBH5调控的RIG-1通过IKKε/TBK1/IRF3通路影响IFNα的分泌
已有研究报道RIG-1识别病毒RNA,激活IKKε/TBK1/IRF3通路诱导I型干扰素产生。为了探究ALKBH5是否也通过调控RIG-I来影响IFNα的分泌,检测了RIG-I和IFNα产生的下游信号通路。有趣的是, GSEA分析显示,ALKBH5沉默后RIG-1样受体通路和干扰素α/β信号通路显著富集,表明ALKBH5参与了RIG-I信号转导和干扰素的产生。在HNSCC细胞系中,RIG-I过表达后IKKε/TBK1/IRF3磷酸化水平升高,酶联免疫吸附试验显示过表达RIG-I后培养液中IFNα分泌增加。此外,过表达 ALKBH5显著降低了IFNα的分泌,同样,敲低HNRNPC后也降低了IFNα的分泌。为了探索IKKε/TBK1/IRF3通路的作用,使用IKKε/TBK1特异性抑制剂bay985。这种抑制剂降低了ALKBH5敲低后引起的RIG-I表达的上调和IFNα的分泌。
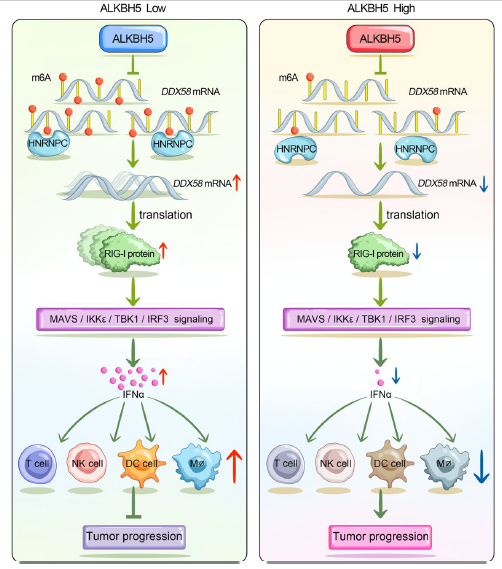
IFNα作为一种免疫调节细胞因子,在自然杀伤细胞(NK)、T细胞、树突状细胞(dc)等免疫细胞的激活中发挥重要作用,并发挥抗肿瘤作用。使用小鼠HNSCC细胞系SCC7在免疫活性C3H/HeJ小鼠体内建立异种移植模型,发现IFNα逆转了ALKBH5过表达介导的促肿瘤能力。过表达ALKBH5后,血清IFNα浓度降低。此外,ALKBH5沉默后,肿瘤浸润淋巴细胞中NK细胞、T细胞、DCs和M1巨噬细胞的百分比显著降低。以上结果表明,HNSCC中过表达ALKBH5可通过调控RIG-I抑制IFNα的分泌,进而抑制免疫浸润,促进肿瘤进展。
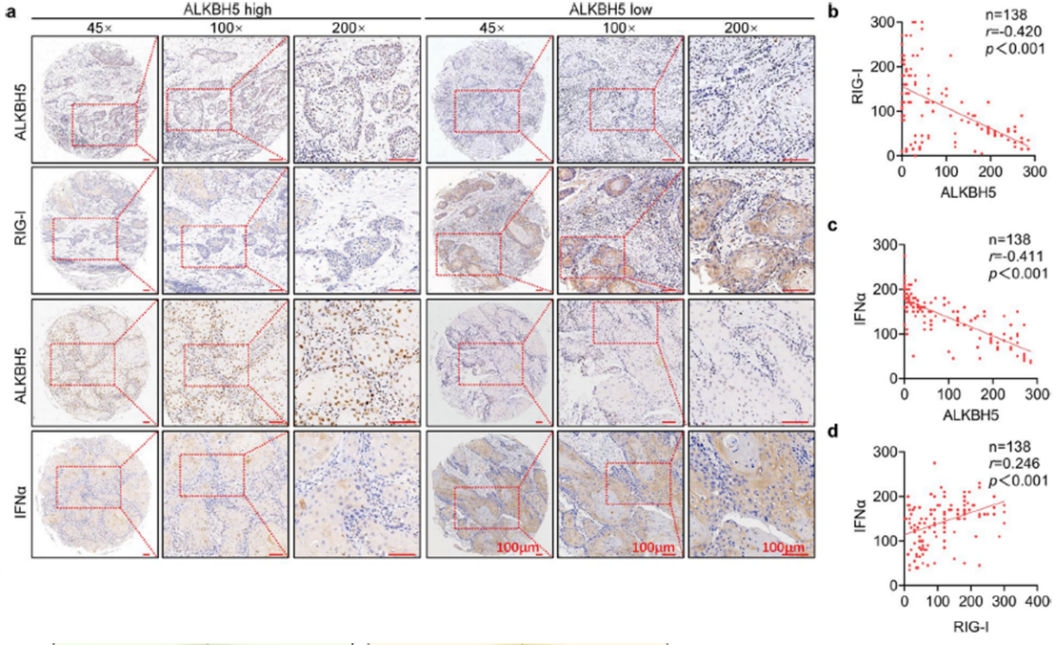
8、AKLBH5表达上调与HNSCC中RIG-1和IFNα表达呈负相关
为了研究ALKBH5/ RIG-I/IFNα调控轴的临床相关性,使用组织芯片对138例HNSCC标本进行了免疫组化染色。ALKBH5的表达与RIG-I和IFNα的蛋白水平呈负相关,而RIG-I的表达与IFNα的表达呈正相关。这些结果在临床样本中验证了相关性。综上所述,上调的ALKBH5通过IKKε/TBK1/ IRF3通路抑制RIG-I介导的IFNα分泌,从而在HNSCC中发挥致癌作用,最终减少免疫杀伤细胞浸润,促进肿瘤进展。
云序生物m6A修饰研究五大模块
01 m6A RNA修饰测序
m6A RNA修饰测序(m6A-meRIP-seq)
对m6A RNA甲基化,目前zui流行的检测手段为m6A-MeRIP-Seq技术,适用于m6A RNA甲基化谱研究,快速筛选m6A RNA甲基化靶基因。云序可提供mRNA和多种非编码RNA的m6A测序:
- m6A 全转录组测序(涵盖mRNA,LncRNA,circRNA)
- m6A LncRNA测序(涵盖LncRNA和mRNA)
- m6A Pri-miRNA测序(涵盖Pri-miRNA和mRNA)
- m6A mRNA测序
- m6A miRNA测序
LC-MS/MS检测整体RNA修饰水平
精准高效,可以实现一次检测,9类修饰水平检测,一步到位。
比色法检测整体RNA修饰水平
快速检测m6A整体甲基化水平
03 m6A RNA修饰上游酶的筛选m6A RNA修饰相关酶PCR芯片
寻找上游直接调控m6A RNA甲基化的甲基转移酶。
04 m6A RNA修饰靶基因验证
MeRIP-qPCR
云序提供各类不同修饰的meRIP-qPCR服务,可针对mRNA,lncRNA,环状RNA等不同类型的RNA分子进行检测,低通量验证RNA修饰靶基因表达水平。
05机制互作研究
5.1 RIP-seq/qPCR
筛选或验证RNA修饰直接靶点,研究RNA修饰靶基因的调控机制。
5.2 RNA pull down -MS/WB
筛选或验证目标RNA互作基因或蛋白,研究相应的分子调控机制。
5.3 双荧光素酶实验
验证两基因互作,研究相应的分子调控机制。
5.4 ChIP-seq
筛选或验证目标蛋白与DNA互作,研究相应的分子调控机制。
优势二:至今完成4000+例 m6A测序样本,全面覆盖医口、农口等各类样本。
优势三:全面检测mRNA和各类非编码RNA(circRNA,lncRNA,Pri-miRNA等)。
优势四:du家提供m6A一站式服务:m6A整体水平检测、m6A测序、MeRIP-qPCR验证、RIP和RNA pull-down等。
优势五:率先研发超微量MeRIP测序技术,RNA量低至500ng起。
优势六:国内最全的RNA修饰测序平台,提供m6A、m5C、m1A、m7G、m3C、m6Am、O8G、ac4C乙酰化和2'-O-甲基化测序。
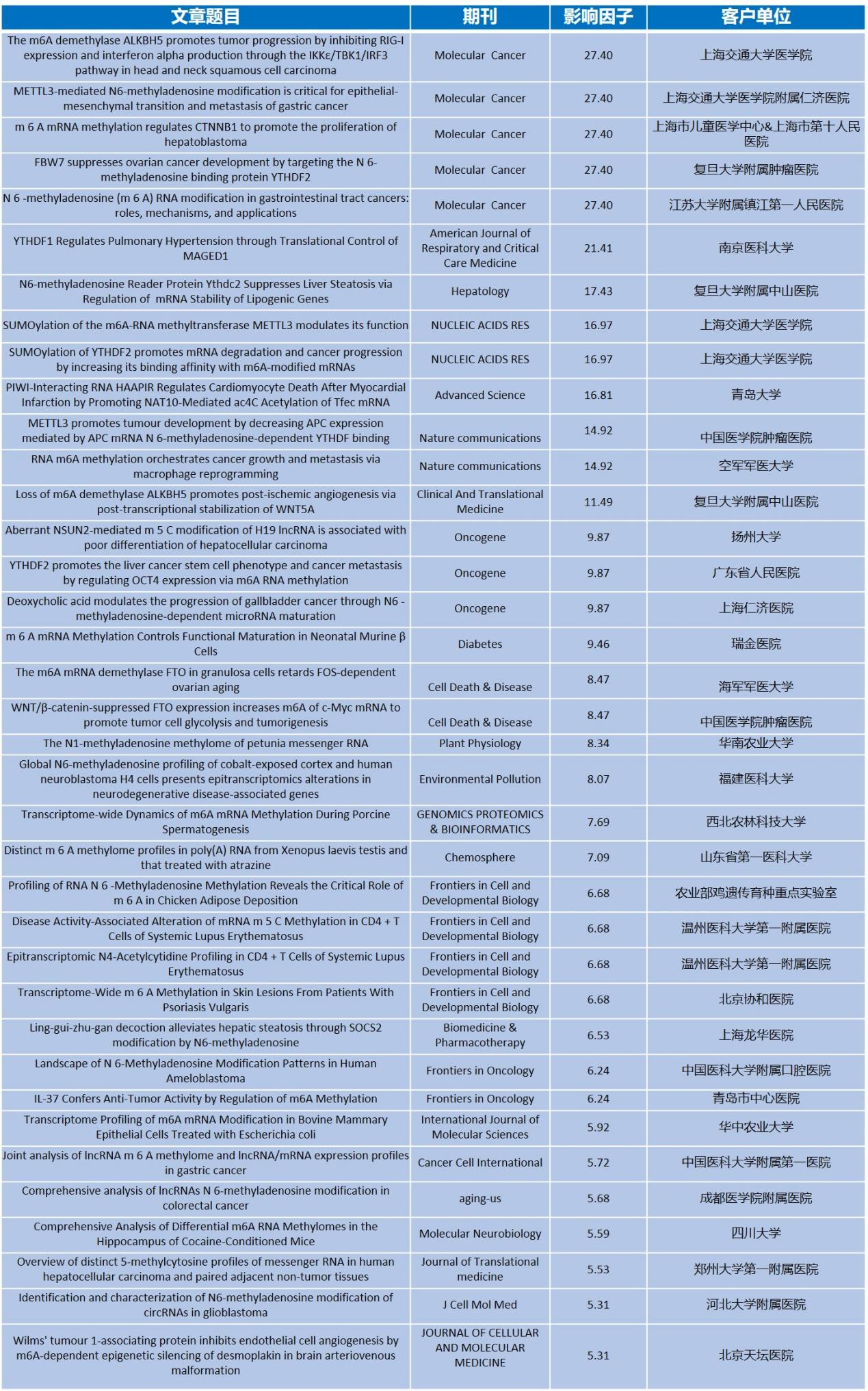
云序客户RNA修饰部分文章列表
相关产品
m6A RNA甲基化测序
m5C RNA甲基化测序
m1A RNA甲基化测序
m7G RNA甲基化测序
ac4C RNA乙酰化测序
O8G RNA氧化修饰测序
2’-O-RNA甲基化测序
m6Am RNA甲基化测序
RNA pulldown
RNA-seq
RIP
往期回顾
时间不够?云序m6A甲基化测序技术助力用户3-5个月发表5分文章!
超详细图文版:如何实现m6A测序数据可视化?
云序生物 | 2021年客户m6A项目文章汇总
9-12月m6Azui新高分文章汇总
1区 IF: 21|云序MeRIP-Seq & RIP-Seq助力肺动脉高压中m6A阅读蛋白YTHDF1机制研究
云序生物zui新“RNA”甲基化研究汇总——m6A修饰之植物篇
云序项目文章纯测序发表7分杂志|西北农林猪精子m6A修饰文章
项目文章|赫捷院士团队揭密肺腺癌 m6A 机制再次登上Nature 子刊!
项目文章|赫捷院士团队nature子刊揭示METTL3以m6A依赖方式调控食管鳞癌
农口方向3个月内搞定5分文章秘籍——m6A热点错不了
m6A项目文章|ALKBH5通过调控WNT5A稳定性促进缺血后血管生成
3-5月 m6A RNA甲基化影响因子10+文章集锦
云序客户再发15分文章:FBW7靶向m6A结合蛋白YTHDF2抑制卵巢癌
Science新发现 |RNA以m6A依赖方式调节染色质状态和基因转录
m6A 10分+文章思路干货视频
Nat Commun | 云序客户揭示Mettl3协调癌症的生长和转移的分子机制
项目文章|m6A甲基化修饰对神经退行性疾病的重大发现
云序客户余健秀课题组m6A方向再次取得重大发现——SUMO化促进YTHDF2结合m6A修饰的mRNA影响癌症进展
一次RNA甲基化测序,多项成果|云序测序带您超高性价比体验
2020年整年度RNA甲基化文献汇总
9-11月 m6A RNA甲基化影响因子10+文章集锦
项目文章|Nature子刊m6A修饰携手miRNA揭示脱氧胆酸在胆囊癌中作用机制
云序超微量MeRIP测序技术助力用户m6A甲基化文章连续发表
m1A多篇齐发:除了m6A,还有哪些热门RNA修饰?
云序客户zui新成果揭秘:三个月内搞定5分m6A甲基化谱文章?
8月m6A RNA甲基化影响因子10+文章集锦
20分Nature子刊|揭秘神经发育过程中m6A RNA甲基化与组蛋白修饰间的关系
去甲基化酶ALKBH5在胰腺癌中的作用荣登15分杂志
国自然热点—m6A等热门RNA修饰研究技术漫谈




