产品分类
公司荣誉
公司图片
联系方式
公司新闻
3-5月 m6A RNA甲基化影响因子10+文章集锦
发布时间:2021-06-08 14:49 | 点击次数:
N6-甲基腺苷(m6A)修饰是一种普遍存在且有重要生物学功能的RNA化学修饰。细胞内几乎所有类型的RNA分子中均广泛存在m6A修饰。RNA分子m6A修饰状态的动态变化及其功能主要由m6A甲基转移酶(Writer)、m6A去甲基化酶(Eraser)和m6A阅读蛋白(Reader,即“读码器”)等蛋白复合物共同调控。N6-甲基腺苷修饰(m6A)作为目前发现的生物体内丰富的RNA修饰之一,受到众多研究者关注的热点。 近些年来关于m6A研究的文章以惊人的速度上升,CNS期刊不断报道,就近2021年3-5月发表的m6A相关研究文章已达240多篇,其中10分以上文章达到40多篇。 今天小编就m6A修饰近3个月的高分热点进行解析,带大家把握m6A修饰新方向。
3-5月10+以上文章汇总
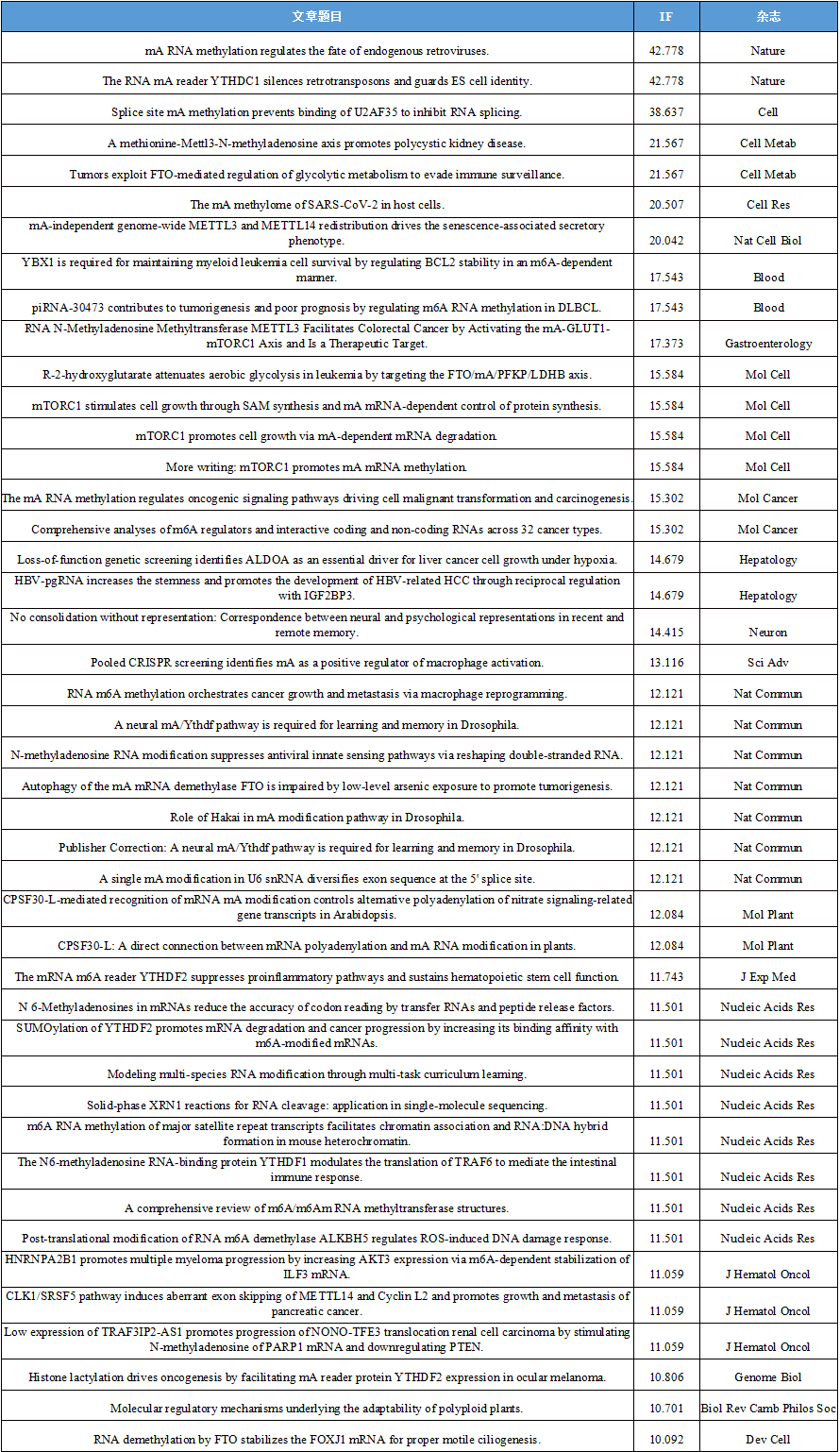
高分案例
1.m6A RNA甲基化调控内源性逆转录病毒的命运文章链接:m6A RNA methylation regulates the fate of endogenous retroviruses
发表杂志:Nature
发表日期:2021.03
影响因子:42.778
摘要:内源性逆转录病毒(ERVs)是丰富的异质整合逆转录病毒序列组,在其以RNA为中心的生命周期中影响基因组调控和细胞生理过程。本文中作者在小鼠胚胎干细胞中使用CRISPR敲除筛选,确定了m6A RNA甲基化可作为限制ERVs的一种方法。ERV mRNA的甲基化是由甲基转移酶Mettl3-Mettl14蛋白复合物催化的,Mettl3-Mettl14及其附属亚基WTAP和ZC3H13的缺失通过靶向5 '非翻译区域导致了IAPs和ERVK元件相关mRNA丰度的增加。通过控制生长素依赖性METTL3-METTL14酶复合物的降解,发现IAP mRNA和蛋白丰度与m6A呈动态负相关。通过监测染色质状态和METTL3-METTL14双敲后mRNA的稳定性,发现m6A甲基化主要通过减少IAP mRNA的半衰期而起作用,这是通过招募m6A阅读蛋白的YTHDF家族发生的。上述结果表明,RNA甲基化通过清除EVA来源的RNA物种,在维持细胞完整性中提供了保护,这可能在转录沉默不那么严格的情况下尤为重要。
2.RNA m6A阅读蛋白YTHDC1可以抑制逆转录转座子并保护ES细胞的身份
文章链接:The RNA m6A reader YTHDC1 silences retrotransposons and guards ES cell identity
发表杂志:Nature
发表日期:2021.03
影响因子:42.778
摘要:N6-甲基腺苷(m6A)在许多生物过程中起着关键作用。然而,人们对m6A在哺乳动物早期发育阶段的作用仍知之甚少。研究表明,m6A阅读蛋白YTHDC1以m6A依赖的方式维持小鼠胚胎干细胞(ES)所必需的,其缺失可启动细胞重编程至2C-like状态。在机制上,在小鼠ES细胞中YTHDC1结合到逆转录转座子的转录本上(如颅内A粒子,ERVK和LINE1)及其缺失导致这些沉默的逆转录转座子重新激活,同时setdb1介导H3K9me3三甲基化整体减少。进一步发现YTHDC1及其靶m6A RNA在SETDB1上游作用,抑制逆转录转座子和Dux。本研究揭示了m6A RNA和YTHDC1在染色质修饰和逆转录转座子抑制中的重要作用。
3.剪切位点的m6A修饰阻止U2AF35结合从而抑制RNA剪切
文章链接:Splice site m6A methylation prevents binding of U2AF35 to inhibit RNA splicing
发表杂志:Cell
发表日期:2021.04.27
影响因子:38.637
摘要:N6-methyladenosine (m6A) RNA修饰被广泛用于改变mRNA的命运。本文中作者证明了秀丽隐杆线虫的甲基化修饰蛋白METT-10(小鼠mettl16的同源蛋白)沉积在s -腺苷甲硫氨酸(SAM)合成酶前体mRNA的3’剪接位点(AG)上的一个m6A修饰,可抑制其正确剪接和蛋白产生。这种机制是由丰富的饮食触发的,以m6A介导的开关来停止SAM的产生并调节其内稳态。虽然哺乳动物SAM合成酶pre-mRNA不受此机制调控,但3’剪接位点m6A修饰抑制剪切在哺乳动物中是保守的。该修饰通过物理方式阻止必要的剪接因子U2AF35识别3’剪接位点。作者认为使用剪切位点m6A修饰是一种古老的剪接调节机制。
4. 蛋氨酸-Mettl3-m6A轴促进多囊肾病
文章链接:A methionine-Mettl3-N6-methyladenosine axis promotes polycystic kidney disease
发表杂志:Cell Metabolism
发表日期:2021.04.09
影响因子:21.567
摘要:常染色体显性多囊肾病(ADPKD)是一种常见的单基因疾病,以大量进行性增大的肾囊肿为特征。Mettl3是一个m6A修饰酶,被发现与发育相关,而其在大多数疾病中的作用尚未可知。本文中作者发现小鼠和人类ADPKD样本中Mettl3和m6A水平升高,肾脏特异性转基因Mettl3表达导致管状囊肿。相反,在三个同源ADPKD小鼠模型中,Mettl3的缺失会减缓囊肿的生长。有趣的是,在ADPKD模型中蛋氨酸和s -腺苷甲硫氨酸(SAM)水平也升高。此外,蛋氨酸和SAM诱导了Mettl3的表达并加剧了体外囊肿的生长,而限制蛋氨酸饮食则使ADPKD小鼠的生长减弱。最后,Mettl3通过增强的c-Myc和Avpr2 mRNA m6A修饰和翻译激活促进囊肿的c-Myc和cAMP通路。因此,Mettl3促进ADPKD,并将蛋氨酸的利用与表观组学激活增殖和囊肿生长联系起来。
5.肿瘤利用糖酵解代谢中FTO介导的调控来逃避免疫监视
文章链接:Tumors exploit FTO-mediated regulation of glycolytic metabolism to evade immune surveillance
发表杂志:Cell Metabolism
发表日期:2021.04.21
影响因子:21.567
摘要:越来越多的了解复杂的因素和调节机制,有助于免疫逃避促进免疫疗法的发展。然而,恶性肿瘤的多样性限制了许多在特定的遗传和表观遗传背景下已知的机制,表明寻找常规的驱动基因是十分必要的。本文中作者发现m6A去甲基化酶FTO是肿瘤通过糖酵解代谢调节来逃避免疫监视的一个必要的表观调控因子。研究表明,FTO介导的肿瘤细胞m6A去甲基化可提高转录因子C-Jun、JunB和C/EBPβ的水平,从而重新运行糖酵解代谢。Fto敲低会降低肿瘤细胞的糖酵解活性,恢复CD8+ T细胞的功能,从而抑制肿瘤生长。此外,作者还开发了一种小分子化合物Dac51,它可以抑制FTO的活性,阻断FTO介导的免疫逃逸以更好地控制肿瘤,这表明RNA表观转录组是一种潜在的免疫治疗策略。
6. 宿主细胞中SARS-CoV-2的m6A甲基化组
文章链接:The m6A methylome of SARS-CoV-2 in host cells
发表杂志:Cell Research
发表日期:2021.04
影响因子:20.507
摘要:新急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)因其快速传播和高死亡率已导致全球卫生紧急事件。宿主与病毒基因组RNA相互作用的分子机制尚不清楚。本文发现SARS-CoV-2基因组RNA在人类和猴子细胞中被m6A动态修饰。结合RIP-seq和miCLIP分析,在基因组中共鉴定出8个单碱基分辨率的m6A位点。那些被鉴定为m6A修饰的突变菌株通过聚类分析表明已经在美国形成了一个独特的分类。进一步功能实验表明,m6A甲基化负调控SARS-CoV-2感染。SARS-CoV-2感染也引发了寄主整体m6A水平的增加,表现为mRNA中m6A的定位和motif的改变。总之,上述结果表明m6A作为一个动态的表观转录组标志介导病毒与寄主互作。
7. 不依赖m6A的全基因组Mettl3和Mettl14再分配驱动了与衰老相关的分泌表型
文章链接:m6A-independent genome-wide METTL3 and METTL14 redistribution drives the senescence-associated secretory phenotype
发表杂志:Nature Cell Biology
发表日期:2021.04
影响因子:20.042
摘要:Mettl3和Mettl14是催化mRNA m6A修饰的甲基转移酶复合物的核心亚基。尽管甲基转移酶复合物中依赖m6A的功能越来越多,但METTL3和METTL14复合物不依赖m6A的功能仍然鲜为人知。本文中作者发现Mettl3和Mettl14的全基因组再分配以m6A独立的方式转录驱动衰老相关分泌表型(SASP)。Mettl14被重新分配到增强子中,而Mettl3在衰老过程中定位于SASP基因启动子中已存在的NF-κB位点。Mettl3和Mettl14是SASP所必需的。然而,SASP不受mRNA m6A修饰的调控。METTL3和METTL14在小鼠模型体内由SASP介导的衰老细胞促肿瘤和免疫监测功能中都是必需的。总之,上述结果说明METTL3和METTL14复合物以不依赖m6A修饰的方式在衰老过程中转录促进SASP。
云序生物m6A修饰研究五大模块
01 m6A RNA修饰测序
m6A RNA修饰测序(m6A-meRIP-seq)
对m6A RNA甲基化,目前流行的检测手段为m6A-Seq技术,适用于m6A RNA甲基化谱研究,快速筛选m6A RNA甲基化靶基因。云序可提供mRNA和多种非编码RNA的m6A测序:
- m6A 全转录组测序(涵盖mRNA,LncRNA,circRNA)
- m6A LncRNA测序(涵盖LncRNA和mRNA)
- m6A Pri-miRNA测序(涵盖Pri-miRNA和mRNA)
- m6A mRNA测序
- m6A miRNA测序
LC-MS/MS检测整体RNA修饰水平
精准高效,可以实现一次检测,9类修饰水平检测,一步到位。
比色法检测整体RNA修饰水平
快速检测m6A整体甲基化水平
03 m6A RNA修饰上游酶的筛选
m6A RNA修饰相关酶PCR芯片
寻找上游直接调控m6A RNA甲基化的甲基转移酶。
04 m6A RNA修饰靶基因验证
meRIP-qPCR
云序提供各类不同修饰的meRIP-qPCR服务,可针对mRNA,lncRNA,环状RNA等不同类型的RNA分子进行检测,低通量验证RNA修饰靶基因表达水平。
05机制互作研究
5.1 RIP-seq/qPCR
筛选或验证RNA修饰直接靶点,研究RNA修饰靶基因的调控机制。
5.2 RNA pull down -MS/WB
筛选或验证目标RNA互作基因或蛋白,研究相应的分子调控机制。
5.3 双荧光素酶实验
验证两基因互作,研究相应的分子调控机制。
5.4 ChIP-seq
筛选或验证目标蛋白与DNA互作,研究相应的分子调控机制。
云序生物服务优势:
优势一:发表10分以上文章zui多的m6A RNA甲基化测序服务平台。云序已累计支持客户发表44篇高水平文章,合计影响因子300分+,是国内支持发文zui多、累计影响因子zui高的公司。
优势二:至今完成4000+例 m6A测序样本,覆盖医口、农口等各类样本。
优势三:检测mRNA和各类非编码RNA(circRNA,lncRNA,Pri-miRNA等)。
优势四:提供m6A一站式服务:m6A整体水平检测、m6A测序、MeRIP-qPCR验证、RIP和RNA pull-down。
优势五:率先研发超微量meRIP测序技术,RNA量低至500ng起。
优势六:国内zui全的RNA修饰测序平台,提供m6A、m5C、m1A、m7G、m3C、O8G、ac4C乙酰化和2'-O-甲基化测序。
云序客户RNA修饰文章列表
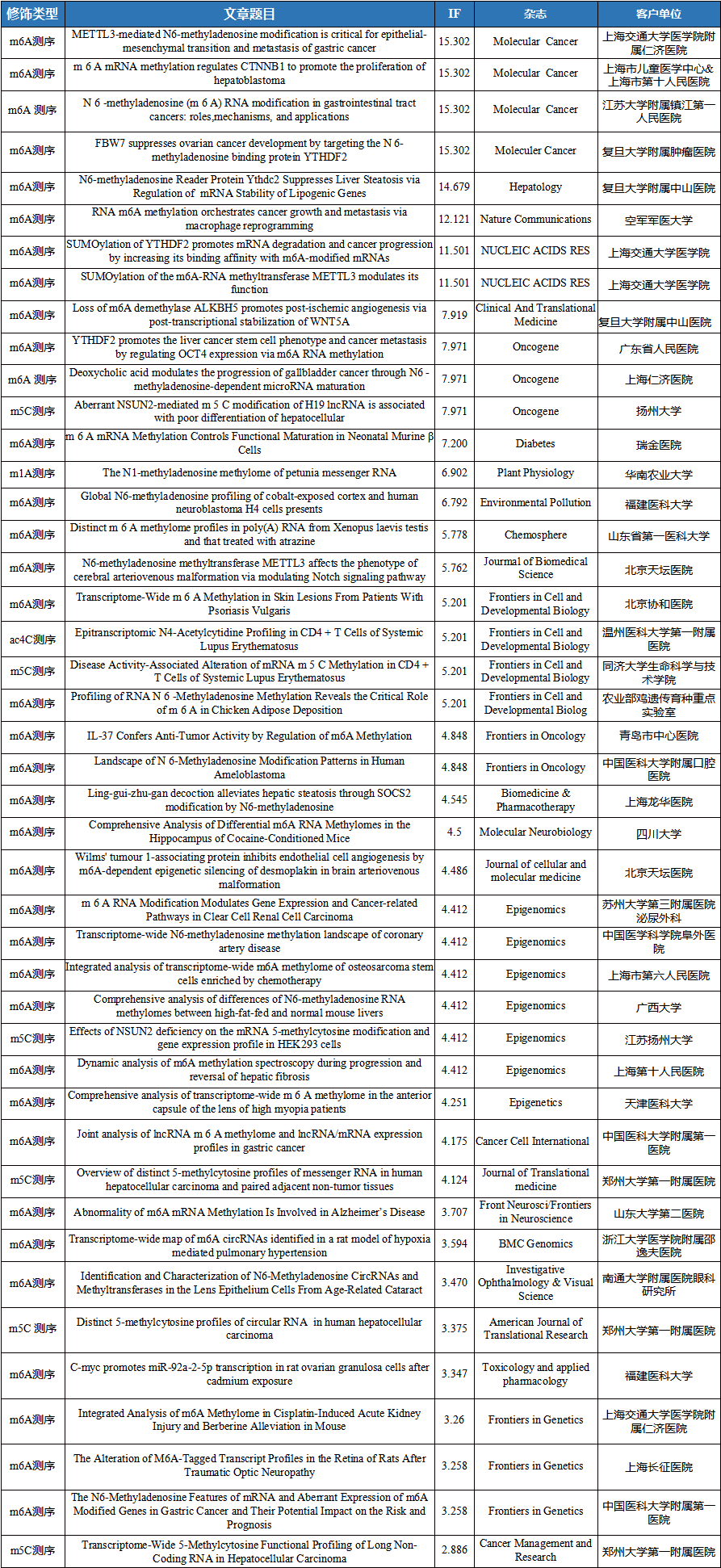
相关产品:
m1A RNA甲基化测序
m5C RNA甲基化测序
m7G (m3C)RNA 甲基化测序
2’-O-RNA氧化测序
ac4C乙酰化测序
o8G RNA氧化测序
比色法/LC-MS检测整体m6A甲基化水平
RNA修饰相关酶PCR芯片
ATAC-seq
ChIP-seq
往期回顾
云序客户再发15分文章:FBW7靶向m6A结合蛋白YTHDF2抑制卵巢癌
Science新发现 |RNA以m6A依赖方式调节染色质状态和基因转录
m6A 10分+文章思路干货视频
Nat Commun | 云序客户揭示Mettl3协调癌症的生长和转移的分子机制
项目文章|m6A甲基化修饰对神经退行性疾病的重大发现
云序客户余健秀课题组m6A方向再次取得重大发现——SUMO化促进YTHDF2结合m6A修饰的mRNA影响癌症进展
一次RNA甲基化测序,多项成果|云序测序带您超高性价比体验
2020年整年度RNA甲基化文献汇总
9-11月 m6A RNA甲基化影响因子10+文章集锦
m5C新高分汇总|带你直击m5C研究前沿
云序用户文章|Nature子刊揭示LncRNA发生m5C异常修饰或成肝癌诊断新靶点
项目文章|Nature子刊m6A修饰携手miRNA揭示脱氧胆酸在胆囊癌中作用机制
云序超微量MeRIP测序技术助力用户m6A甲基化文章连续发表
m1A多篇齐发:除了m6A,还有哪些热门RNA修饰?
云序客户新成果揭秘:三个月内搞定5分m6A甲基化谱文章?
云序4篇项目文章|m5C RNA修饰表达谱文章教您如何另辟蹊径快速发文
ac4C荣登Nature:RNA修饰研究大有可为
8月m6A RNA甲基化影响因子10+文章集锦
20分Nature子刊|揭秘神经发育过程中m6A RNA甲基化与组蛋白修饰间的关系
去甲基化酶ALKBH5在胰腺癌中的作用荣登15分杂志
国自然热点—m6A等热门RNA修饰研究技术漫谈

上海云序生物科技有限公司
Shanghai Cloud-seq Biotech Co., Ltd.
地址:上海市松江区莘砖公路518号20号楼3楼
电话:021-64878766
传真:021-64878766
网址:www.cloud-seq.com.cn
邮箱:market@cloud-seq.com.cn




