云序客户余健秀课题组m6A方向再次取得重大发现——SUMO化促进YTHDF2结合m6A修饰的mRNA影响癌症进展
发布时间:2021-02-22 15:47 | 点击次数:
前言
2021年2月12日上海交通大学医学院余健秀课题组再次携手云序生物MeRIP-seq,RIP-seq等技术在Nucleic Acids Research上发表了文章SUMOylation of YTHDF2 promotes mRNA degradation and cancer progression by increasing its binding affinity with m6A-modified mRNAs,针对YTHDF2与m6A修饰展开研究,发现YTHDF2阅读蛋白SUMO化会影响其结合m6A修饰mRNA的能力,促进mRNA降解,从而调控癌细胞的生长。这是继2018年余健秀课题组首次通过云序生物MeRIP-seq技术在Nucleic Acids Research上发表了文章SUMOylation of the m6A-RNA methyltransferase METTL3 modulates its function,以及2020年通过云序生物MeRIP技术以及microRNA测序技术在Oncogene上面发表了文章Deoxycholic acid modulates the progression of gallbladder cancer through N6-methyladenosine-dependent microRNA maturation之后又一新力作。下面我们一起来看看这篇文章的研究思路和成果。
文章导读



发表日期:2020.2.12
发表杂志:Nucleic Acids Research
应用技术:RIP-seq, m6A-MeRIP-seq,mRNA-seq
文章链接:SUMOylation of YTHDF2 promotes mRNA degradation and cancer progression by increasing its binding affinity with m6A-modified mRNAs
文章内容
1. m6A阅读蛋白YTHDF2上的SUMO化修饰
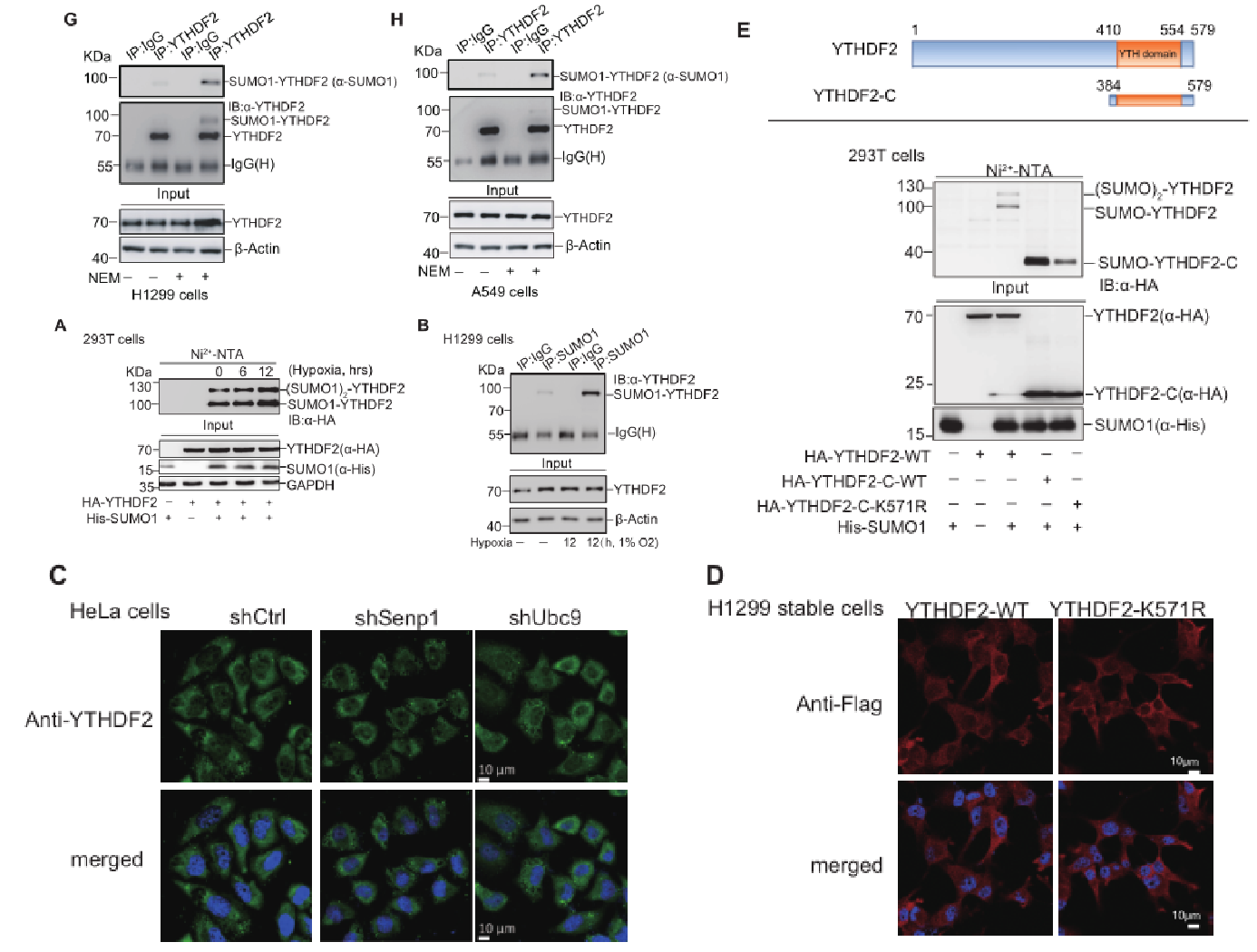
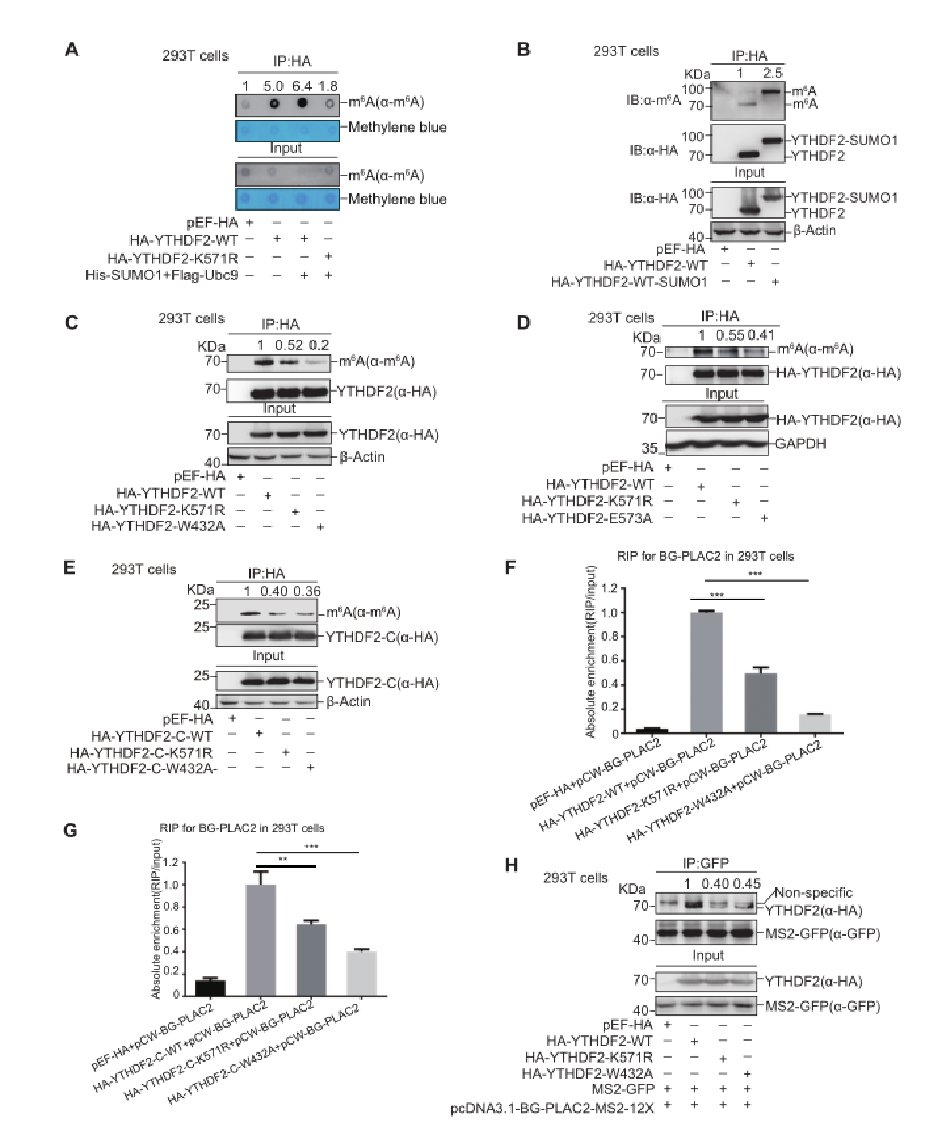
作者利用构建质粒转染、RIP后点杂交实验检测YTHDF2结合的m6A修饰的mRNA量,通过对比YTHDF2-WT和空质粒发现YTHDF2能与m6A修饰的mRNA结合,通过对比YTHDF2-WT和YTHDF2-K571R以及对比HA-YTHDF2-SUMO和HA-YTHDF2等,发现SUMO化的YTHDF2与m6A修饰的mRNA的结合力增强。
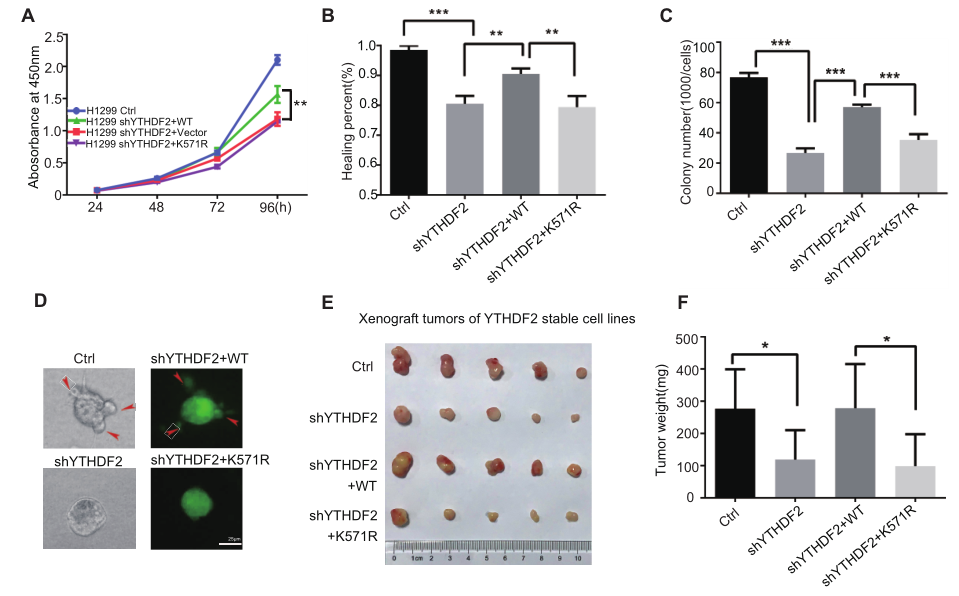
通过沉默内源YTHDF2的表达再引入外源 YTHDF2-WT和YTHDF2-K571R来调控 H1299细胞内的SUMO化YTHDF2,进行细胞实验发现,YTHDF2的SUMO化对癌细胞的侵袭能力至关重要。异种肿瘤移植实验也证实了YTHDF2的SUMO化促进肿瘤生长。
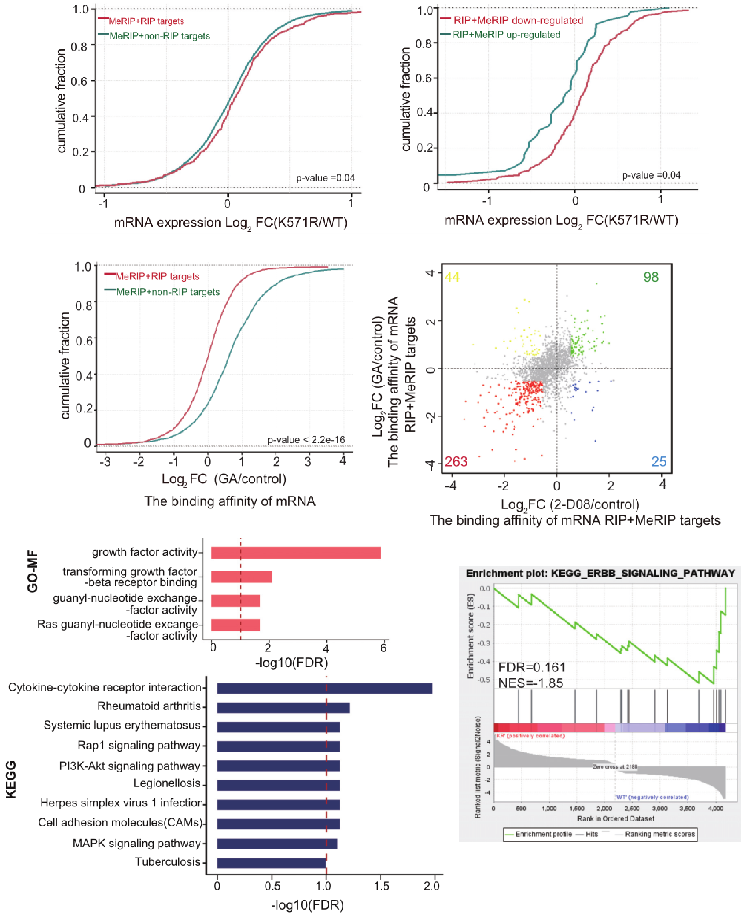
为了进一步挖掘YTHDF2阅读蛋白SUMO化是如何影响癌症发展的,作者通过RIP-seq检测与YTHDF2结合的基因,通过m6A-MeRIP-seq检测发生m6A修饰的基因,两部分结果联合分析发现,在带有m6A修饰的基因中,与YTHDF2结合的基因明显在突变的YTHDF2-K571 R细胞中以及在YTHDF2 SUMO化抑制的细胞中结合力减弱。细胞实验证实YTHDF2的结合会降低结合基因的表达。mRNA-seq显示YTHDF2的结合基因在YTHDF2-K571 R细胞中表达明显上升。GO、KEGG和GSEA分析显示,结合YTHDF2并且在YTHDF2 SUMO化的细胞中表达也下降的基因,功能富集在生长因子活性、鸟苷酸交换因子活性等相关条目,而分析显示在YTHDF2 SUMO化的细胞中表达上升的基因则在肺癌相关通路富集。对TCGA数据库中的数据分析显示,在YTHDF2高表达的患者中,SUMO1高表达与不良预后相关。
总结
这篇文章利用RIP-seq、m6A-MeRIP-seq和mRNA-seq联合分析探究了SUMO化对YTHDF2结合m6A修饰的mRNA的能力的影响和结合后对mRNA的调控,揭示了m6A阅读蛋白YTHDF2促进癌症发展的新机制。
作者介绍
上海交通大学医学院侯国芳博士、赵娴副研究员为该论文的共同第一作者,余健秀研究员、上海交通大学医学院附属第九人民医院肿瘤科主任姜斌教授为共同通讯作者。
余健秀:现任上海交通大学医学院PI、特聘教授、博士生导师、生物化学与分子细胞学系科研副主任。余健秀研究组一直致力于从事与肿瘤相关的蛋白质修饰(PTMs)和RNA修饰功能机制的研究。尤其近年来,在蛋白质修饰调控RNA修饰及代谢作用机制方面取得了一些创新性成果。
云序m6A RNA修饰课题技术服务
五大模块
1.m6A RNA修饰测序
MeRIP-seq
通过使用m6A抗体富集高甲基化的RNA片段,然后结合高通量测序,在全转录组范围内研究发生m6A的区域
2.m6A RNA修饰靶基因验证
MeRIP-qPCR
云序提供m6A的MeRIP-qPCR服务,可针对mRNA,lncRNA,环状RNA等不同类型的RNA分子进行检测,低通量验证m6A修饰靶基因表达水平。
3.机制互作研究
RIP-seq/qPCR
筛选或验证m6A修饰直接靶点,研究m6A修饰靶基因的调控机制。
RNA pull down -MS/WB
筛选或验证目标RNA互作基因或蛋白,研究相应的分子调控机制。
双荧光素酶实验
验证两基因互作,研究相应的分子调控机制。
4.RNA修饰上游酶的筛选
RNA修饰相关酶PCR芯片
寻找上游直接调控m6A甲基化的甲基转移酶。
5.检测整体m6A RNA修饰水平
LC-MS/MS检测整体RNA修饰水平
精准高效,可以实现一次检测,9类修饰水平检测,一步到位。
比色法检测整体m6A甲基化水平
周期短、RNA起始量小,低至200ng。




